题目内容
10.下列有关物质的性质与其应用不相对应的是( )| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 | |
| B. | 氯气具有强氧化性,因此可用于漂白有色布料 | |
| C. | NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏 | |
| D. | 氢氟酸能与二氧化硅反应,因此可用于刻蚀玻璃 |
分析 A.依据浓硫酸具有强氧化性能够使铁、铝发生钝化;
B.氯气不具有氧化性;
C.氨气与氯气反应生成氯化铵固体;
D.氢氟酸与二氧化硅反应生成四氟化硅和水.
解答 解:A.浓硫酸具有强氧化性能够使铁、铝发生钝化形成致密氧化膜,可以组织反应进行,所以可在常温下用铝制容器贮藏贮运浓硫酸,故A正确;
B.氯气不具有氧化性,不能漂白有色布料,故B错误;
C.氨气与氯气反应生成氯化铵固体,产生大量白盐,可以可用浓氨水检验输送氯气的管道是否有泄漏,故C正确;
D.氢氟酸与二氧化硅反应生成四氟化硅和水,能够腐蚀玻璃,用于刻蚀玻璃,故D正确;
故选:B.
点评 本题考查了元素化合物知识,侧重考查物质的性质与用途,熟悉相关物质的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
11.下列有关物质分类或归类正确的是( )
①混合物:漂白粉、水玻璃、Fe(OH)3胶体、冰水混合物
②化合物:CaCl2、NaOH、HCl、HT
③同素异形体:C60、碳纳米管、金刚石、石墨
④电解质:胆矾、苛性钠、冰醋酸、氧化钾
⑤煤的干馏、煤的汽化和液化都属于化学变化
⑥硅酸盐:光导纤维、水晶、玻璃、水玻璃.
①混合物:漂白粉、水玻璃、Fe(OH)3胶体、冰水混合物
②化合物:CaCl2、NaOH、HCl、HT
③同素异形体:C60、碳纳米管、金刚石、石墨
④电解质:胆矾、苛性钠、冰醋酸、氧化钾
⑤煤的干馏、煤的汽化和液化都属于化学变化
⑥硅酸盐:光导纤维、水晶、玻璃、水玻璃.
| A. | ①②④⑤ | B. | ③④⑤ | C. | ③④⑥ | D. | ①②③④⑤⑥ |
1.下列说法正确的是( )
| A. | 在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,则原溶液中一定有CO32- | |
| B. | 如果某化学反应的△H和△S均小于0,则反应一定能自发进行 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI2 | |
| D. | 一定量氯气通入30mL 10mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
18.下列描述中正确的是( )
| A. | HCN为V形分子 | |
| B. | NO3-的空间构型为三角锥形 | |
| C. | SF6中有6对完全相同的成键电子对 | |
| D. | SO42-和SO32-的中心原子均为sp3杂化 |
5.化合物丙可由如下反应得到C4H10O$→_{△}^{浓H_{2}SO_{4}}$C4H8$→_{溶剂CCI_{4}}^{Br_{2}}$C4H8Br2,丙的结构简式不可能是( )
| A. | CH3CH(CH2Br)2 | B. | (CH3)2BrCH2Br | C. | C2H5CHBrCH2Br | D. | CH3(CHBr)2CH3 |
2.2008年北京奥运会的水立方建筑,采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯.下列说法不正确的是( )
| A. | 四氟乙烯为非极性分子 | |
| B. | 合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应 | |
| C. | 聚全氟乙丙烯的分子结构可能为【-CF2-CF2--CF2-CF--CF3-】 | |
| D. | ETFE中可能存在“-CH2-CH2-CF2-CF2-”的连接方式 |
19.利用如图所示的有机物X可生产S-诱抗素Y.下列说法正确的是
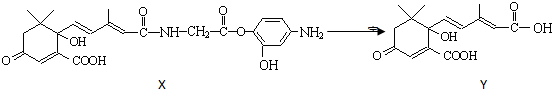 ( )
( )
 ( )
( )| A. | Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 | |
| B. | 1 molY与足量NaOH溶液反应,最多消耗3 mol NaOH | |
| C. | 1 molX最多能加成9 molH2 | |
| D. | X可以发生氧化、取代、酯化、加聚、缩聚反应 |
 ,最简单烯烃的结构简式为
,最简单烯烃的结构简式为 ,最简单芳香烃的分子式为C6H6,C4H10 的一氯代物有4种,C5H12 的同分异构体中沸点最低的物质 的结构简式为
,最简单芳香烃的分子式为C6H6,C4H10 的一氯代物有4种,C5H12 的同分异构体中沸点最低的物质 的结构简式为 .
.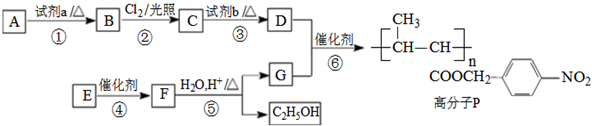
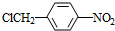 .
.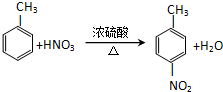 .
.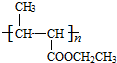 +nH2O$→_{△}^{H+}$
+nH2O$→_{△}^{H+}$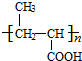 +n CH3CH2OH.
+n CH3CH2OH.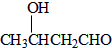 以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).