题目内容
家用液化气的主要成分之一是丁烷.当10kg丁烷完全燃烧并生成二氧化碳和液态水时放出的热量为5×105kJ.又知1mol液态水汽化时需吸收44kJ热量,则1mol丁烷完全燃烧产生气态水时放出的热量为( )
| A、2900kJ |
| B、2680kJ |
| C、3120kJ |
| D、2856kJ |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:依据n=
将丁烷的质量换算成物质的量,结合提供的热量计算2mol丁烷完全反应放出的热量,已知1mol液态水汽化时需要吸收44kJ热量,依据热化学方程式和盖斯定律计算得到1mol丁烷完全燃烧产生气态水时放出的热量.
| m |
| M |
解答:
解:当10kg丁烷完全反应,其物质的量为:n=
=
=
mol,完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,则2mol丁烷完全反应放热=
=5800KJ,其热化学方程式为:2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l)△H=-5800kJ/mol,已知1mol液态水汽化时需要吸收44kJ热量,①H2O(l)=H2O(g)△H=44KJ/mol;②2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l)△H=-5800kJ/mol;
依据盖斯定律①×10+②得到2C4H10(g)+13O2(g)→8CO2(g)+10H2O(g)△H=-5360kJ/mol,则得到反应,C4H10(g)+
O2(g)→4CO2(g)+5H2O(g)△H=-2680KJ/mol;则1mol丁烷完全燃烧产生气态水时放出的热量为2680KJ,
故选B.
| m |
| M |
| 10000g |
| 58g/mol |
| 10000 |
| 58 |
| 2×5×105KJ | ||
|
依据盖斯定律①×10+②得到2C4H10(g)+13O2(g)→8CO2(g)+10H2O(g)△H=-5360kJ/mol,则得到反应,C4H10(g)+
| 13 |
| 2 |
故选B.
点评:本题主要考查了反应热的计算,题目难度不大,注意物质的量与热量成正比是解题的关键.注意焓变计算和物质聚集状态的关系.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
关于Na2CO3和NaHCO3的说法中正确的是( )
| A、为了将Na2CO3固体中的NaHCO3固体除去可以采用加热的方法 |
| B、Na2CO3溶液可以与Ca(OH)2溶液反应,而NaHCO3溶液不可以 |
| C、Na2CO3和NaHCO3都能与CaCl2溶液反应 |
| D、质量相同的Na2CO3 和NaHCO3与足量盐酸反应时所产生的CO2质量也相同 |
正确的实验操作是科学探究成功的基础.下列操作中正确的是( )
A、 取用少量液体 |
B、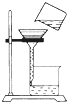 过滤 |
C、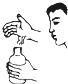 闻气味 |
D、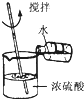 稀释浓硫酸 |
下列化学反应的离子方程式正确的是( )
| A、金属铝溶于氢氧化钠溶液:2Al+6OH-═2[Al(OH)4]-+3H2↑ |
| B、碳酸氢钙溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O |
| C、二氧化硅与足量烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| D、硫酸滴加到氢氧化钡溶液中:H++OH-═H2O |
下列反应的离子方程式书写正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O | ||||
| C、硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | ||||
D、除去KNO3溶液中的Fe3+:Fe3++3H2O
|
已知0.1mol/L H2A、NaHA溶液的pH分别为3.5、8.5,现有下列6种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①Na2A与HCl;②NaHA与NaOH;③NaOH与NH4Cl;④Na2A与NaHA;⑤Na2A与NaOH;⑥NaHA与HCl.下列各项排序正确的是( )
| A、pH:⑤>③>④>②>①>⑥ |
| B、c(A2-):⑤>②>④>①>⑥>③ |
| C、溶液中c(H+):⑥>①>④>②>③>⑤ |
| D、c(H2A):⑥>④>①>②>⑤>③ |
下列各组物质中,都是共价化合物的是( )
| A、H2S和Na2O2 |
| B、H2O2和CaF2 |
| C、NH3和N2 |
| D、HNO3和HClO3 |
下列有关叙述正确的是( )
| A、等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| B、pH=4.5的柠檬汁中c(H+)是pH=6.5的番茄汁中c(H+)的100倍 |
| C、100mL pH=3的HA溶液、HB溶液分别与足量的锌反应,HA溶液放出的氢气较多,说明HA的酸性比HB的强 |
| D、pH=5.5的CH3COOH与CH3COONa混合溶液中:c(Na+)>c(CH3COO-) |