题目内容
下面关于电解质的叙述中正确的是( )
| A、液态硫酸不导电,硫酸是非电解质 |
| B、NaHSO4在熔融状态下电离产生Na+和HSO4-两种离子 |
| C、溶于水后能导电的化合物一定是电解质 |
| D、电解质在电流的作用下电离产生离子 |
考点:电解质与非电解质
专题:
分析:A.电解质导电的条件是水溶液或熔融状态;
B.NaHSO4在熔融状态下电离产生Na+和HSO4-两种离子;
C.根据电解质定义分析;
D.电解质电离的条件是水溶液或熔融状态.
B.NaHSO4在熔融状态下电离产生Na+和HSO4-两种离子;
C.根据电解质定义分析;
D.电解质电离的条件是水溶液或熔融状态.
解答:
解:A.电解质导电的条件是水溶液或熔融状态,硫酸在水溶液中电离出氢离子和硫酸根离子,能导电,属于强电解质,故A错误;
B.NaHSO4在熔融状态下电离产生Na+和HSO4-两种离子,故B正确;
C.电解质自身能电离出自由移动离子,溶于水能导电的化合物,不一定是自身电离,如氨气溶于水和水结合成一水合氨,一水合氨电离,一水合氨是电解质,氨气是非电解质,故C错误;
D.电解质电离的条件是水溶液或熔融状态,与电流无关,故D错误;
故选B.
B.NaHSO4在熔融状态下电离产生Na+和HSO4-两种离子,故B正确;
C.电解质自身能电离出自由移动离子,溶于水能导电的化合物,不一定是自身电离,如氨气溶于水和水结合成一水合氨,一水合氨电离,一水合氨是电解质,氨气是非电解质,故C错误;
D.电解质电离的条件是水溶液或熔融状态,与电流无关,故D错误;
故选B.
点评:电解质必须具备下列条件,缺一不可:1、必须是化合物,2、在水溶液里或熔融状态下有自由移动的离子,且离子是物质本身电离的,不能是与其它物质反应后的物质电离的.注意NaHSO4在熔融状态下电离和在水溶液中电离不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
地壳中含量最多的元素是( )
| A、Al | B、Si | C、Fe | D、O |
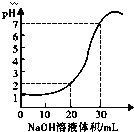 如图为10mL x mol?L-1的盐酸用y mol?L-1的NaOH溶液滴定的图象,依据图象推出x和y的数值可能是下列各组中的( )
如图为10mL x mol?L-1的盐酸用y mol?L-1的NaOH溶液滴定的图象,依据图象推出x和y的数值可能是下列各组中的( )| A | B | C | D | |
| x | 0.12 | 0.04 | 0.03 | 0.09 |
| y | 0.04 | 0.12 | 0.09 | 0.03 |
| A、A | B、B | C、C | D、D |
关于
C的说法正确的是( )
| 12 |
| 6 |
| A、质量数为6 |
| B、质子数为6 |
| C、电子数为13 |
| D、中子数为6 |

 与1分
与1分 在一定条件下可发生类似反应①的反应,生成有机化合物Ⅵ,Ⅵ的结构简式为
在一定条件下可发生类似反应①的反应,生成有机化合物Ⅵ,Ⅵ的结构简式为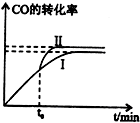 二甲醚是一种重要的清洁燃料,有多种合成方法.
二甲醚是一种重要的清洁燃料,有多种合成方法.