题目内容
20.下列事实中,不能用勒夏特列原理加以解释的是( )| A. | 醋酸溶液加水稀释醋酸的电离程度增大 | |
| B. | 工业合成氨时常用通过过量的氮气的方法提高氢气的转化率 | |
| C. | 新制的氯水在光照的条件下颜色变浅 | |
| D. | 氯化铁溶液中加Fe粉振荡后颜色变浅 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.加水稀释醋酸,醋酸浓度降低,则醋酸根离子和氢离子结合速率降低,所以促进醋酸电离,可以用平衡移动原理解释,故A不选;
B.合成氨时,加入过量氮气,平衡向正反应方向移动,则提高氢气转化率,可以用平衡移动原理解释,故B不选;
C.新制的氯水中存在化学平衡,CL2+H2O?HCl+HClO,在光照条件下次氯酸见光分解,平衡正向进行,溶液颜色变浅,能用勒夏特列原理解释,故C不选;
D.氯化铁中加入Fe粉时,二者反应生成氯化亚铁,不存在平衡移动,所以不能用平衡移动原理解释,故D选;
故选D.
点评 本题考查化学平衡移动原理,为高频考点,注意:平衡移动原理适用于改变条件能引起平衡移动的可逆反应,为易错题.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
11.利用如图所示装置模拟电解原理在工业生产上的应用.下列说法中正确的是( )
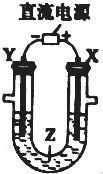

| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的Cu2+浓度变小 | |
| C. | 制取金属镁时,Z是熔融的氧化镁 | |
| D. | 在铁片上镀铜时,Y是纯铜 |
8.有八种物质:①甲烷 ②苯 ③聚丙烯 ④聚1,3-丁二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯 ⑧裂解气,既能使KMnO4酸性溶液褪色,又能与溴水反应褪色的是( )
| A. | ③④⑤⑥⑦⑧ | B. | ④⑤⑧ | C. | ④⑤⑦⑧ | D. | ③④⑤⑧ |
15.下列叙述正确的是( )
| A. | 在醋酸溶液中加入少量NaHSO4固体,醋酸的电离平衡左移,且溶液中的c(H+)减小 | |
| B. | 加热蒸干并灼烧硝酸铝溶液,最终得到的固体是Al(NO3)3 | |
| C. | 常温下,将 pH=1的醋酸溶液稀释1000倍,测得 pH=4 | |
| D. | 熵增加且放热的反应一定是自发反应 |
5.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质,并用来生产ZnSO4•6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的 pH 如下表.
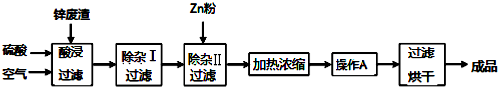
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+.为使 Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.为控制上述pH范围可选择加入的试剂或药品是AD.
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)常温下,已知 Ksp[Zn(OH)2]=5×10-17,某 ZnSO4溶液里c(Zn2+)=0.5mol/L,如果要生成Zn(OH)2沉淀,则应调整溶液 pH 大于6.
(4)当向含相同浓度Cu2+、Fe3+、Fe2+的溶液中滴加某浓度的NaOH溶液时,Fe3+(填离子符号)先沉淀,Ksp[Fe(OH)2]>Ksp[Cu(OH)2](填“>”、“=”或“<”)

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的 pH | 3.3 | 1.5 | 6.5 | 5.4 | 4.2 |
| 沉淀完全的 pH | 5.2 | 3.7 | 9.7 | 8.0 | 6.7 |
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+.为使 Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.为控制上述pH范围可选择加入的试剂或药品是AD.
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)常温下,已知 Ksp[Zn(OH)2]=5×10-17,某 ZnSO4溶液里c(Zn2+)=0.5mol/L,如果要生成Zn(OH)2沉淀,则应调整溶液 pH 大于6.
(4)当向含相同浓度Cu2+、Fe3+、Fe2+的溶液中滴加某浓度的NaOH溶液时,Fe3+(填离子符号)先沉淀,Ksp[Fe(OH)2]>Ksp[Cu(OH)2](填“>”、“=”或“<”)
12.在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
| A. | K+、AlO2-、Cl-、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ca2+、Fe2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
9.能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案是( )
| A. | 取a克混合物充分加热至质量不变,减重b克 | |
| B. | 取a克混合物与足量稀硝酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体 | |
| C. | 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰完全吸收,增重b克 | |
| D. | 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
 在通常状况下,A为固态单质.根据下图转化关系,回答:
在通常状况下,A为固态单质.根据下图转化关系,回答: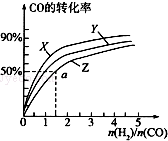 甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1