题目内容
标准状况下,ag气体A和bg气体B的分子数相同,下列说法不正确的是( )
| A、气体A和B的相对分子质量之比为 a:b |
| B、同质量的气体A和B所含分子数目之比为b:a |
| C、标准状况下,气体A和B的密度之比为b:a |
| D、相同条件下,等体积的气体A和B的质量之比为a:b |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:标况下,气体摩尔体积相等,ag气体A和bg气体B的分子数相同,说明二者的物质的量相等,则A、B的摩尔质量之比等于其质量之比=a:b,
A.气体分子摩尔质量在数值上等于其相对分子质量;
B.根据N=
NA知,相同质量时其分子数之比等于摩尔质量的反比;
C.标况下,气体摩尔体积相等,根据ρ=
知,其密度之比等于摩尔质量之比;
D.相同条件下,气体摩尔体积相等,等体积的气体其物质的量相等,再根据m=nM计算其质量之比.
A.气体分子摩尔质量在数值上等于其相对分子质量;
B.根据N=
| m |
| M |
C.标况下,气体摩尔体积相等,根据ρ=
| M |
| Vm |
D.相同条件下,气体摩尔体积相等,等体积的气体其物质的量相等,再根据m=nM计算其质量之比.
解答:
解:标况下,气体摩尔体积相等,ag气体A和bg气体B的分子数相同,说明二者的物质的量相等,则A、B的摩尔质量之比等于其质量之比=a:b,
A.气体分子摩尔质量在数值上等于其相对分子质量,所以其相对分子质量之比为a:b,故A正确;
B.根据N=
NA知,相同质量时其分子数之比等于摩尔质量的反比=b:a,故B正确;
C.标况下,气体摩尔体积相等,根据ρ=
知,其密度之比等于摩尔质量之比=a:b,故C错误;
D.相同条件下,气体摩尔体积相等,等体积的气体其物质的量相等,再根据m=nM知,相同物质的量时其质量之比等于摩尔质量之比=a:b,故D正确;
故选C.
A.气体分子摩尔质量在数值上等于其相对分子质量,所以其相对分子质量之比为a:b,故A正确;
B.根据N=
| m |
| M |
C.标况下,气体摩尔体积相等,根据ρ=
| M |
| Vm |
D.相同条件下,气体摩尔体积相等,等体积的气体其物质的量相等,再根据m=nM知,相同物质的量时其质量之比等于摩尔质量之比=a:b,故D正确;
故选C.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,侧重考查灵活运用能力,熟练掌握基本公式,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
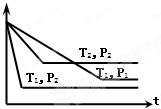 已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )| A、T1>T2,P1>P2,m+n>x,正反应放热 |
| B、T1<T2,P1<P2,m+n<x,正反应吸热 |
| C、T1>T2,P1<P2,m+n<x,正反应放热 |
| D、T1<T2,P1>P2,m+n>x,正反应吸热 |
X、Y、Z为短周期元素,这些元素原子的最外层电子数分别为1、4、6,则由这三种元素组成的化合物的化学式可能是( )
| A、XYZ |
| B、X3YZ |
| C、XYZ2 |
| D、X2YZ3 |
由如图分析,有关叙述正确的是( )
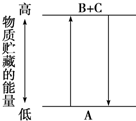

| A、A-→B+C和B+C-→A两个反应吸收或放出的能量不等 |
| B、A-→B+C是放热反应 |
| C、A具有的能量高于B和C具有的能量总和 |
| D、A-→B+C是吸热反应,则B+C-→A必然是放热反应 |
下列说法正确的是( )
| A、在标准状况下,1mol水的体积是22.4L |
| B、1molH2所占的体积一定是22.4L |
| C、在标准状况下,NA个任何分子所占的体积约为22.4L |
| D、在标准状况下,28g的N2体积约为22.4L |
同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳,下列说法正确的是( )
| A、所含分子数和质量均不相同 |
| B、含有相同的分子数和电子数 |
| C、含有相同的质子数和中子数 |
| D、含有相同数目的中子、原子和分子 |
下列各组离子中,在溶液中能大量共存 的是( )
| A、Na+、Ca2+、CO32- |
| B、Na+、Ca2+、HCO3- |
| C、H+、SO42-、OH- |
| D、H+、Na+、CO32- |
在一定温度下向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应X(g)+Y(g)?2Z(g),此反应达到平衡的标志是( )
| A、容器内压强不随时间变化 |
| B、容器内各物质的浓度不随时间变化 |
| C、容器内X、Y、Z的浓度之比为1:1:2 |
| D、单位时间内消耗0.1 mol X同时生成0.2 mol Z |