题目内容
5.向500mL CuSO4和Fe2(SO4)3的混合溶液中加入16.8g铁粉,充分反应后,经过滤、洗涤、干燥,可得6.4g铜.要使SO42-完全沉淀,需加入2.0mol/L BaCl2溶液500mL.求:(1)溶液中SO42-的物质的量浓度;
(2)原混合溶液中CuSO4的物质的量.
分析 (1)发生SO42-+Ba2+=BaSO4↓,结合n=cV计算;
(2)可得6.4g铜,先发生Fe+2Fe3+=3Fe2+、后发生Fe+Cu2+=Fe2++Cu,结合反应及电荷守恒计算.
解答 解:(1)n(BaCl2)=0.5L×2mol/L=1mol,由SO42-+Ba2+=BaSO4↓可知,原溶液中n(SO42-)=1mol,则溶液中SO42-的物质的量浓度为$\frac{1mol}{0.5L}$=2mol/L,
答:溶液中SO42-的物质的量浓度为2mol/L;
(2)n(Fe)=$\frac{16.8g}{56g/mol}$=0.3mol,n(Cu)=$\frac{6.4g}{64g/mol}$=0.1mol,由Fe+Cu2+=Fe2++Cu可知,参加反应的Fe为0.1mol,则0.2molFe与Fe2(SO4)3反应,由Fe+2Fe3+=3Fe2+可知,c(Fe3+)=$\frac{0.4mol}{0.5L}$=0.8mol/L,又原溶液不显电性,设原混合溶液中CuSO4的物质的量浓度为x,则x×2+0.8×3=2×2,解得x=0.8mol/L,可知原混合溶液中CuSO4的物质的量为0.8mol/L×0.5L=0.4mol,
答:原混合溶液中CuSO4的物质的量为0.4mol.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、物质的量关系、氧化的先后顺序、电荷守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.氢氧燃料电池已用于航天飞机,它是以铂作电极,H2SO4溶液作电解质,正极反应为:O2+4H++4e-=2H2O,负极反应为:2H2-4e-=4H+.下列叙述不正确的是( )
| A. | H2在负极发生氧化反应 | B. | 燃料电池的能量转化率可达100% | ||
| C. | 是一种高效、环境友好的发电装置 | D. | 供电时的总反应为:2H2+O2=2H2O |
13.下列事实能说明氨水是弱电解质的是( )
| A. | 氨水与氯化铝溶液反应产生氢氧化铝沉淀 | |
| B. | 用氨水做导电实验,灯泡很暗 | |
| C. | 0.1mol/L的氨水的pH<13 | |
| D. | 氯化铵溶液的pH<7 |
20.下列实验操作正确的是( )
| A. | 制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加入几片碎瓷片 | |
| B. | 稀释浓硫酸时,常把水加入到盛浓硫酸的烧杯中 | |
| C. | 做CO还原Fe2O3实验时,为防止CO污染环境,实验完毕,常先停止通CO,再停止加热 | |
| D. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
1.下列离子方程式书写正确是( )
| A. | 硫酸溶液与氢氧化钡溶液反应:Ba2++H++OH-+SO42-═BaSO4↓+H2O | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3NH3•H2O══Al(OH)3↓+3NH4+ | |
| C. | Na与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 碳酸钠与氢氧化钠:HCO3-+OH-═CO32-+H2O |
5.下列关于“化学与健康”的说法不正确的是( )
| A. | 服用铬含量超标的药用胶囊会对人体健康造成危害 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 | |
| D. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 |
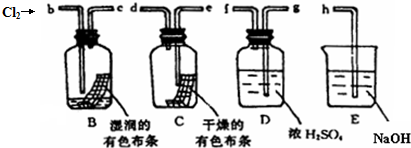
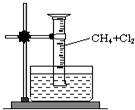 某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白: