题目内容
(1)有下列八种物质:①MgCl2晶体 ②干冰 ③NaOH晶体 ④白磷(P4)晶体 ⑤金刚石 ⑥硼晶体,其中属于离子晶体的是 ;属于分子晶体的是 ,属于原子晶体的是 .
(2)SO2的分子构型为 ,请从分子构型的角度分析SO2、CO2在水中溶解度的差别 .
(2)SO2的分子构型为
考点:判断简单分子或离子的构型,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:(1)由阴阳离子构成的晶体属于离子晶体,由分子构成的晶体属于分子晶体,由原子构成的晶体属于原子晶体,根据晶体的构成微粒判断晶体类型;
(2)根据价层电子对互斥理论确定分子空间构型,根据相似相溶原理分析物质的溶解性.
(2)根据价层电子对互斥理论确定分子空间构型,根据相似相溶原理分析物质的溶解性.
解答:
解:(1)①MgCl2晶体是由镁离子和氯离子构成的,为离子晶体;
②干冰是由二氧化碳分子构成的,为分子晶体;
③NaOH晶体是由钠离子和氢氧根离子构成的,为离子晶体;
④白磷(P4)晶体是由分子构成的,为分子晶体;
⑤金刚石是由原子构成的,为原子晶体;
⑥硼晶体是由原子构成的,为原子晶体,
所以属于离子晶体的是①③;属于分子晶体的是②④,属于原子晶体的是⑤⑥,故答案为:①③;②④;⑤⑥;
(2)二氧化硫分子中价层电子对个数=2+
×(6-2×2)=3且含有一个孤电子对,所以为V形结构,SO2是V形的极性分子,CO2是直线型的非极性分子,根据相似相溶原理,SO2在水中的溶解度比CO2的大,故答案为:V形;SO2是V形的极性分子,CO2是直线型的非极性分子,根据相似相溶原理,SO2在水中的溶解度比CO2的大.
②干冰是由二氧化碳分子构成的,为分子晶体;
③NaOH晶体是由钠离子和氢氧根离子构成的,为离子晶体;
④白磷(P4)晶体是由分子构成的,为分子晶体;
⑤金刚石是由原子构成的,为原子晶体;
⑥硼晶体是由原子构成的,为原子晶体,
所以属于离子晶体的是①③;属于分子晶体的是②④,属于原子晶体的是⑤⑥,故答案为:①③;②④;⑤⑥;
(2)二氧化硫分子中价层电子对个数=2+
| 1 |
| 2 |
点评:本题考查了晶体类型的判断、分子的空间构型及相似相溶原理等知识点,根据晶体的构成微粒确定晶体类型,根据价层电子对互斥理论确定微粒空间构型,题目难度不大.

练习册系列答案
相关题目
已知葡萄糖的燃烧热是2804kJ/mol,当它氧化生成1g 液态水时放出的热量是( )
| A、26.0kJ |
| B、51.9kJ |
| C、155.8kJ |
| D、467.3kJ |
由-CH3、-OH、 、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
 、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有( )| A、1种 | B、2种 | C、3种 | D、4种 |

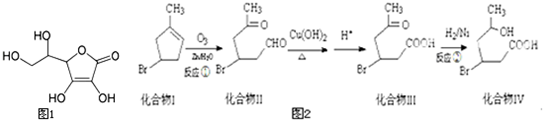
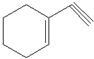 (1)某有机化合物分子结构式如图采取sp2杂化的C原子有
(1)某有机化合物分子结构式如图采取sp2杂化的C原子有 )发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为
)发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为