题目内容
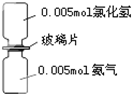 如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )| A、气体反应物的总体积为0.224L |
| B、产物中所含的N-H键个数为0.02NA |
| C、生成物中含有0.005NA个分子 |
| D、加1L水溶解后所得溶液中阳离子浓度为0.005mol?L-1 |
考点:氨的化学性质
专题:氮族元素
分析:A.标况下气体的摩尔体积为22.4L/mol;
B.1个NH4Cl中含有4个N-H;
C.NH4Cl为离子晶体不存在分子;
D.氨根离子水解生成一水合氨.
B.1个NH4Cl中含有4个N-H;
C.NH4Cl为离子晶体不存在分子;
D.氨根离子水解生成一水合氨.
解答:
解:A.氯化氢和氨气的总的物质的量为0.01mol,但是题目没有指明反应的状况为标况,所以气体的摩尔体积不一定为22.4L/mol,故A错误;
B.1个NH4Cl中含有4个N-H,氯化氢和氨气反应生成NH4Cl的物质的量为0.005mol,含N-H键数为0.005×4×NA=0.02NA,故B正确;
C.NH4Cl为离子晶体不存在分子,故C错误;
D.氯化氢和氨气反应生成NH4Cl的物质的量为0.005mol,氨根离子为弱碱阳离子,在水溶液中部分水解,所以溶液中阳离子浓度小于0.005mol?L-1,故D错误;
故选:B.
B.1个NH4Cl中含有4个N-H,氯化氢和氨气反应生成NH4Cl的物质的量为0.005mol,含N-H键数为0.005×4×NA=0.02NA,故B正确;
C.NH4Cl为离子晶体不存在分子,故C错误;
D.氯化氢和氨气反应生成NH4Cl的物质的量为0.005mol,氨根离子为弱碱阳离子,在水溶液中部分水解,所以溶液中阳离子浓度小于0.005mol?L-1,故D错误;
故选:B.
点评:本题考查了氨气的性质,题目难度不大,D选项为易错项,解题时应考虑到氨根离子的水解.

练习册系列答案
相关题目
下列说法正确的是( )
| A、糖类、油脂、蛋白质都是高分子化合物,它们水解的最终产物不相同 |
| B、检验溴乙烷中的溴元素,可以在溴乙烷中加入AgNO3溶液 |
| C、葡萄糖在一定条件下能水解生产乙醇与二氧化碳 |
| D、苯酚能与溴水反应,苯不能与溴水反应,说明羟基对苯环有影响 |
下列有关阿伏伽德罗常数说法正确的是( )
| A、含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA |
| B、标况下,22.4L四氯化碳所含分子数大于NA |
| C、0.1mol/L 的AgNO3溶液中,阳离子所带正电荷数目为0.1NA |
| D、标准状况下,11.2L HF含有的HF分子数为0.5NA |
下列判断中,正确的是( )
| A、工业上常通过电解熔融的MgO冶炼金属镁 |
| B、将NaOH溶液逐滴加入FeCl3溶液可制备Fe(OH)3胶体 |
| C、牡丹籽油是一种优良的植物油脂,它可使酸性高锰酸钾溶液褪色 |
| D、溴水不能区别四种有机溶剂:苯、四氯化碳、己烯、无水乙醇 |
已知H2CO3的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11.向0.1mol/L NaOH溶液中通入CO2,若溶液的pH=10(不考虑溶液的体积变化),则下列说法正确的是( )
| A、2c(CO32-)+c(HCO3-)=0.1mol/L | ||||
B、
| ||||
| C、该溶液中加BaCl2溶液,溶液pH增大 | ||||
| D、在溶液中加水,使体积扩大到原来的10倍,则溶液pH明显变小 |
下列说法正确的是( )
| A、不锈钢是铁合金,只含有金属元素 |
| B、木糖醇(C5H10O5)是一种甜味剂,它属于多羟基化合物,与葡萄糖是同分异构体 |
| C、蛋白质在体内经消化后生成碳酸、硫酸、尿酸等,故它属于酸性食物 |
| D、氟氯代烷化学性质稳定,在紫外线照射下分解出氯原子参与破坏臭氧层的反应 |
下面不属于居室污染物的是( )
A、 消毒液、药皂 |
B、 尼古丁、二氧化氮 |
C、 甲醛、二甲苯 |
D、 一氧化碳、二氧化硫 |
下列有关说法错误的是( )
| A、为保护海轮的船壳,常在船壳上镶入锌块 |
| B、纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应 |
| C、已知工业合成氨气△H<0,达平衡后,升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| D、Na2O2与水反应中,氧化剂还原剂都是Na2O2,且1mol Na2O2参加反应有1mol电子转移 |
咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为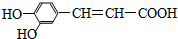 .有关咖啡酸的说法中不正确的是( )
.有关咖啡酸的说法中不正确的是( )
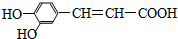 .有关咖啡酸的说法中不正确的是( )
.有关咖啡酸的说法中不正确的是( )| A、咖啡酸可以发生还原、取代、加聚等反应 |
| B、咖啡酸与FeCl3溶液可以发生显色反应 |
| C、1 mol咖啡酸可与4 mol H2发生加成反应 |
| D、1 mol咖啡酸最多能消耗3 mol的NaHCO3 |