题目内容
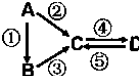 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:(1)若A是当前最常用的太阳能转换为电能的材料.C的水溶液俗称水玻璃,D为硅酸.则:写出反应②的化学方程式
(2)若A是应用最广泛的金属.反应①、⑤均用盐酸,D物质是红褐色.则:
写出反应③的化学方程式
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2.则:反应②的离子方程式为
考点:无机物的推断
专题:推断题
分析:A、B、C、D均为中学化学常见的纯净物,A是单质,
(1)若A是当前最常用的太阳能转换为电能的材料,C的水溶液俗称水玻璃,D为硅酸,则A为Si,C为Na2SiO3,B为SiO2,反应②为Si与氢氧化钠反应转化为硅酸钠与氢气;
(2)若A是应用最广泛的金属,反应①、⑤均用盐酸,D物质是红褐色,则A为Fe,B为FeCl2,C为FeCl3,D为C为Fe(OH)3;
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2,则D为Al(OH)3,C为偏铝酸盐,A为Al,B为氧化铝.
(1)若A是当前最常用的太阳能转换为电能的材料,C的水溶液俗称水玻璃,D为硅酸,则A为Si,C为Na2SiO3,B为SiO2,反应②为Si与氢氧化钠反应转化为硅酸钠与氢气;
(2)若A是应用最广泛的金属,反应①、⑤均用盐酸,D物质是红褐色,则A为Fe,B为FeCl2,C为FeCl3,D为C为Fe(OH)3;
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2,则D为Al(OH)3,C为偏铝酸盐,A为Al,B为氧化铝.
解答:
解:A、B、C、D均为中学化学常见的纯净物,A是单质,
(1)若A是当前最常用的太阳能转换为电能的材料,C的水溶液俗称水玻璃,D为硅酸,则A为Si,C为Na2SiO3,B为SiO2,反应②为Si与氢氧化钠反应转化为硅酸钠与氢气,反应方程式为:Si+2NaOH+H2O=Na2SiO3+2H2↑,
故答案为:Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2NaOH=Na2SiO3+H2O;
(2)若A是应用最广泛的金属,反应①、⑤均用盐酸,D物质是红褐色,则A为Fe,B为FeCl2,C为FeCl3,D为C为Fe(OH)3,则:
反应③是氯化亚铁与氯气反应生成氯化铁,化学方程式为:2FeCl2+Cl2=2FeCl3,FeCl2溶液中加入NaOH溶液的现象是:开始生成白色沉淀,迅速变为灰绿色,最终变为红褐色,沉淀颜色发生变化对应的化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:2FeCl2+Cl2=2FeCl3;开始生成白色沉淀,迅速变为灰绿色,最终变为红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2,则D为Al(OH)3,C为偏铝酸盐,A为Al,B为氧化铝,则:反应②的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,反应④的离子方程式为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-.
(1)若A是当前最常用的太阳能转换为电能的材料,C的水溶液俗称水玻璃,D为硅酸,则A为Si,C为Na2SiO3,B为SiO2,反应②为Si与氢氧化钠反应转化为硅酸钠与氢气,反应方程式为:Si+2NaOH+H2O=Na2SiO3+2H2↑,
故答案为:Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2NaOH=Na2SiO3+H2O;
(2)若A是应用最广泛的金属,反应①、⑤均用盐酸,D物质是红褐色,则A为Fe,B为FeCl2,C为FeCl3,D为C为Fe(OH)3,则:
反应③是氯化亚铁与氯气反应生成氯化铁,化学方程式为:2FeCl2+Cl2=2FeCl3,FeCl2溶液中加入NaOH溶液的现象是:开始生成白色沉淀,迅速变为灰绿色,最终变为红褐色,沉淀颜色发生变化对应的化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:2FeCl2+Cl2=2FeCl3;开始生成白色沉淀,迅速变为灰绿色,最终变为红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2,则D为Al(OH)3,C为偏铝酸盐,A为Al,B为氧化铝,则:反应②的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,反应④的离子方程式为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-.
点评:本题考查无机物推断,涉及Al、Si、Fe元素化合物性质,需要学生熟练掌握元素化合物性质,难度中等.

练习册系列答案
相关题目
实验是研究化学的基础,如图中所示的实验方法、装置或操作均正确的是( )
A、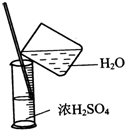 浓硫酸稀释 |
B、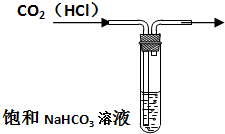 除去CO2中混有的杂质气体(HCl) |
C、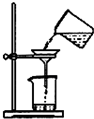 分离出AgNO3溶液中的AgCl |
D、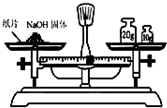 称量32.6g的NaOH固体 |
食品中加入营养强化剂是为了补充食品中缺乏的营养成分或微量元素.下列说法中不正确的是 ( )
| A、人体缺碘,可通过食用加碘盐补碘 |
| B、亚硝酸盐可常用作腌制肉类食品的防腐剂,大量进食易致癌 |
| C、维生素或钙、硒等不能添加在食品中 |
| D、缺铁性贫血,可通过食用铁强化酱油预防. |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 物质 选项 | 甲 | 乙 | 丙 |
| A | AlCl3 | NH3?H2O | NaAlO2 |
| B | NaOH | (NH4)2SO3 | H2SO4 |
| C | SiO2 | NaOH | HF |
| D | CO2 | Ca(OH)2 | Na2CO3 |
| A、A | B、B | C、C | D、D |
下列物质既能与盐酸溶液又能与NaOH溶液反应的是( )
| A、AlCl3 |
| B、NaHCO3 |
| C、Mg |
| D、NH4Cl |
某不纯的铁片可能含有Mg、Al、Cu等金属杂质的一种或几种,取该铁片样品5.6g与足量的稀硫酸反应,得到标准状况下的H2 2.24L,则下列分析的结论中,正确的是( )
| A、一定同时含有三种金属杂质 |
| B、一定不含有杂质铜 |
| C、一定含有杂质镁 |
| D、可能同时含有杂质镁、铝或其中一种 |
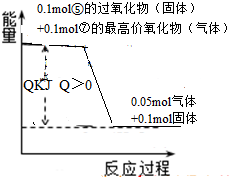
已知:2H2(g)+O2(g)=2H2O(g)△H1
3H2(g)+Fe2O3(s)=2Fe(s)+3H2O(g)△H2
2Fe(s)+
O2(g)=Fe2O3(s)△H3
2Al(s)+
O2(g)=Al2O3(s)△H4
2Al(s)+Fe2O3(s)=A12O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
3H2(g)+Fe2O3(s)=2Fe(s)+3H2O(g)△H2
2Fe(s)+
| 3 |
| 2 |
2Al(s)+
| 3 |
| 2 |
2Al(s)+Fe2O3(s)=A12O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A、△H1<0,△H3>0 |
| B、△H5<0,△H4<△H3 |
| C、△H1=△H2+△H3 |
| D、△H3=△H4+△H5 |
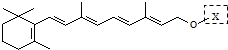 .分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(
.分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(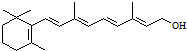 )和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
)和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生