题目内容
9.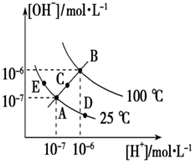 已知水的电离平衡曲线如图所示,试回答下列问题:
已知水的电离平衡曲线如图所示,试回答下列问题:(1)图中A、B、C、D四点的KW 由大到小的顺序B>C>A=D.
(2)若从A点到D点,可采用的方法是加入酸或加入水解显酸性的盐.
(3)在100℃时,将pH=2的硫酸与pH=12的KOH溶液混合至呈中性,需硫酸和氢氧化钾的体积比为100:1.
分析 (1)水的离子积常数只与温度有关,温度越高,离子积常数越大;
(2)从A点到D点c(H+)变大,c(OH-)变小,但Kw不变;
(3)在100℃时,水的离子积为10-12,故pH=12的KOH溶液中c(H+)=10-12mol/L,则c(OH-)=$\frac{1{0}^{-12}}{1{0}^{-12}}$=1mol/L,pH=2的硫酸中c(H+)=10-2mol/L,设需要的硫酸的体积为xL,KOH的体积为yL,根据溶液混合呈中戏时需有:n(H+)=n(OH-)来分析计算.
解答 解:(1)水的离子积常数只与温度有关,温度越高,离子积常数越大,同一曲线是相同温度,根据图知,温度高低点顺序是B>C>A=D,所以离子积常数大小顺序是B>C>A=D,故答案为:B>C>A=D;
(2)在A点时,c(H+)=c(OH-),溶液显中性,而到D点c(H+)变大,c(OH-)变小,溶液显酸性,即由A点到D点,溶液由中性变为酸性,但Kw不变,故可以通过向溶液中加入酸或加入强酸弱碱盐来实现,故答案为:加入酸或加入水解显酸性的盐;
(3)在100℃时,水的离子积为10-12,故pH=12的KOH溶液中c(H+)=10-12mol/L,则c(OH-)=$\frac{1{0}^{-12}}{1{0}^{-12}}$=1mol/L,pH=2的硫酸中c(H+)=10-2mol/L,设需要的硫酸的体积为xL,KOH的体积为yL,根据溶液混合呈中戏时需有:n(H+)=n(OH-)可知:0.01mol/L×xL=1mol/L×yL,解得$\frac{x}{y}$=100:1,故答案为:100:1.
点评 本题考查酸碱混合的定性判断和溶液PH的有关计算,题目难度中等,注意酸碱混合时酸碱物质的量的关系以及溶液PH与c(H+)、(OH-)的关系.

 阅读快车系列答案
阅读快车系列答案| A. | 等物质的量的N2和CO所含分子数均为NA | |
| B. | 1.7g H2O2中含有的电子数为0.9 NA | |
| C. | 1mol Na2O2固体中含离子总数为4 NA | |
| D. | 标准状况下,2.24L戊烷所含分子数为0.1 NA |
| A. | NaCO3 | B. | 氨水 | C. | NH4Cl | D. | NaNO3 |

| A. | OE段表示反应速率最快 | |
| B. | EF段表示反应速率最快,收集的CO2最多 | |
| C. | FG段表示收集的CO2最多 | |
| D. | OG段表示随着时间的推移,反应速率逐渐增快 |
| A. | 46 g钠与氧气完全反应生成Na2O和Na2O2,转移电子数可能为3NA | |
| B. | 向含2 mol FeI2的溶液中通入足量Cl2,消耗氯气分子数为NA | |
| C. | 2 mol Cu与足量硫粉完全反应,转移电子数为2NA | |
| D. | 1 mol Al2Fe(SO4)4固体中含Fe3+的数目为NA |

| A. | a和b用导线连接时,该装置为原电池,铁片为负极,发生氧化反应 | |
| B. | a和b用导线连接时,Pt片上发生的反应为:Cu2++2e-═Cu | |
| C. | a和b分别连接直流电源正、负极时,该装置为电解池,Pt片为阳极,电极反应式为:4OH--4e-═O2↑+2H2O | |
| D. | a和b分别连接直流电源正、负极时,Cu2+向Pt电极移动 |
| A. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Cu与浓硝酸反应制 NO2:Cu+4HNO3(浓)═Cu2++2 NO3-+NO2↑+2H2O | |
| C. | 向同浓度的NaOH和Na2CO3,的混合液中加少量稀盐酸:CO32-+2H+═CO2↑+3H2O | |
| D. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
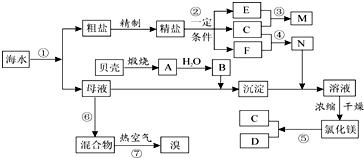

 .
. .
.