题目内容
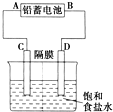 如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).已知:铅蓄电池在放电时发生下列电极反应:负极Pb+SO42--2e-═PbSO4
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).已知:铅蓄电池在放电时发生下列电极反应:负极Pb+SO42--2e-═PbSO4正极PbO2+4H++SO42-+2e-═PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为
(3)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1.15g/cm3)时,
①若铅蓄电池消耗H2SO42mol,则可收集到H2的体积(标准状况下)为
②若消耗硫酸amol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)
考点:电解原理
专题:电化学专题
分析:(1)惰性电极电极饱和食盐水生成氢气、氯气和氢氧化钠,原子守恒配平写出;
(2)电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色说明C电极为阳极,电源A为正极;
(3)①依据电解氯化钠生成氯气电极反应计算转移电子物质的量;
②依据铅蓄电池和电解池中电子转移守恒计算;
③依据铅蓄电池电极反应计算消耗硫酸转移电子,电解过程中电子守恒,根据电解氯化钠溶液的化学方程式计算电解后溶液中溶质和溶液质量得到氢氧化钠的质量分数;
(2)电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色说明C电极为阳极,电源A为正极;
(3)①依据电解氯化钠生成氯气电极反应计算转移电子物质的量;
②依据铅蓄电池和电解池中电子转移守恒计算;
③依据铅蓄电池电极反应计算消耗硫酸转移电子,电解过程中电子守恒,根据电解氯化钠溶液的化学方程式计算电解后溶液中溶质和溶液质量得到氢氧化钠的质量分数;
解答:
解:(1)惰性电极电极饱和食盐水生成氢气、氯气和氢氧化钠,反应的化学方程式为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑;
(2)电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色说明C电极为阳极,D为阴极,电源A为正极,故答案为:正极;
(3)①蓄电池消耗H2SO4 2mol,依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗2mol硫酸电子转移2mol,电解食盐水阴极电极反应2H++2e-=H2↑转移电子2mol生成氢气1mol,标准状况体积为22.4L,则可收集到H2的体积22.4L,
故答案为:22.4;
②依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗amol硫酸电子转移amol,2NaCl+2H2O
2NaOH+Cl2↑+H2↑,反应中转移电子2mol,生成氢氧化钠物质的量为2mol,消耗amol硫酸电子转移amol,生成氢氧化钠amol,氢气0.5amol,氯气0.5amol,得到氢氧化钠溶液的质量分数=
×100%,
故答案为:
×100%.
| ||
故答案为:2NaCl+2H2O
| ||
(2)电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色说明C电极为阳极,D为阴极,电源A为正极,故答案为:正极;
(3)①蓄电池消耗H2SO4 2mol,依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗2mol硫酸电子转移2mol,电解食盐水阴极电极反应2H++2e-=H2↑转移电子2mol生成氢气1mol,标准状况体积为22.4L,则可收集到H2的体积22.4L,
故答案为:22.4;
②依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗amol硫酸电子转移amol,2NaCl+2H2O
| ||
| 40a | ||
1000×1.15-
|
故答案为:
| 40a | ||
1000×1.15-
|
点评:本题考查了原电池,电解池电极分析判断,电极反应中电子守恒计算应用,注意电子守恒的分析判断是解题关键,题目难度中等.

练习册系列答案
相关题目
把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液等体积混合,则混合溶液中微粒浓度关系,正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、2c(H+)=c(CH3COO-)-c(CH3COOH) |
| D、c(CH3COOH)+c(CH3COO-)=0.01mol/L |
天然色素的提取往往应用到萃取操作,现在有用大量水提取的天然色素,下列溶剂不能用来萃取富集这些天然色素的是( )
| A、石油醚 | B、丙酮 | C、乙醇 | D、乙醚 |
下列关于各溶液的描述中正确的是( )
| A、pH相等的①NH4Cl ②(NH4) 2SO4③NH4HSO4的溶液中,c(NH4+)大小:①>②>③ |
| B、向1.00L0.3mol?L-l的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中:3c (Na+)=2[c(HCO3-)+C (CO32-)+c(H2CO3)] |
| C、浓度均为0.1 mol?L-1的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c (CH3COOH)=c (H+)-c(OH-) |
| D、常温下,在l0mL pH=12的氢氧化钠溶液中加入pH=2的HA酸至pH刚好等于7,所得溶液体积V(总)≤20mL |
一定温度下,pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH<a,则该电解质可能是( )
| A、NaCl |
| B、H2SO4 |
| C、CuCl2 |
| D、Na2SO4 |
现用Pt电极电解1L浓度均为0.1mol/L的HCl、CuSO4的混合液,下列说法正确的是( )
| A、电解开始时,阴极有H2放出 |
| B、电解开始时,阳极上发生:Cu2++2e-═Cu |
| C、当电路中通过电子的量超过0.1mol时,阴极放电的种类将发生变化 |
| D、整个电解过程中,SO42-不参加电极反应 |
下列排列顺序正确的是( )
①热稳定性:HF>H2O>NH3 ②离子半径:Na+>Mg2+>F- ③酸性:盐酸>碳酸>醋酸 ④结合质子能力:OH->CO32->HCO3-.
①热稳定性:HF>H2O>NH3 ②离子半径:Na+>Mg2+>F- ③酸性:盐酸>碳酸>醋酸 ④结合质子能力:OH->CO32->HCO3-.
| A、①③ | B、②④ | C、①④ | D、②③ |
下列说法正确的是( )
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、漂白粉的有效成分是CaCl2和Ca(ClO)2,应密封保存 |
| C、欲除去氯气中少量氯化氢气体,可将此混合气体通过盛饱和食盐水的洗气瓶 |
| D、氯水经光照有气泡逸出,该气体为HCl |