题目内容
2.关于相同物质的量浓度的NaHCO3溶液和Na2CO3溶液,下列说法不正确的是( )| A. | 溶液中所含离子的种类相同 | B. | 溶液的pH相同 | ||
| C. | 都能与盐酸反应放出CO2气体 | D. | 都能使澄清石灰水变浑浊 |
分析 A.NaHCO3溶液和Na2CO3溶液都含有钠离子、氢离子、氢氧根离子、碳酸根离子、碳酸氢根离子;
B.碳酸根离子水解能力强于碳酸氢根;
C.碳酸钠、碳酸氢钠都能够与盐酸反应生成氯化钠、水和二氧化碳;
D.碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸氢钙与氢氧化钠反应生成碳酸钙、碳酸钠和水.
解答 解:A.NaHCO3溶液和Na2CO3溶液都含有钠离子、氢离子、氢氧根离子、碳酸根离子、碳酸氢根离子,故A正确;
B.碳酸根离子水解能力强于碳酸氢根,相同物质的量浓度的NaHCO3溶液和Na2CO3溶液,碳酸钠pH大,故B错误;
C.碳酸钠、碳酸氢钠都能够与盐酸反应生成氯化钠、水和二氧化碳,故C正确;
D.碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸氢钙与氢氧化钠反应生成碳酸钙、碳酸钠和水,二者都能产生沉淀碳酸钙,故D正确;
故选:B.
点评 本题考查了碳酸钠与碳酸氢钠的性质,明确二者性质的差别是解题关键,题目难度不大,注意对基础知识的巩固.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
12.某溶液中含有下列离子中的五种:Ba2+、Fe2+、Al3+、Fe3+、Mg2+、HCO3-、CO32-、Cl-、NO3-、SO42-,浓度均为0.1mol/L.向其中加入足量的盐酸,有气体生成且反应后溶液中阴离子的种类没有变化.以下分析错误的是( )
| A. | 原溶液中不含HCO3-和CO32- | |
| B. | 向加盐酸后的溶液中再加KSCN溶液,显红色 | |
| C. | 能确定原溶液中的五种离子 | |
| D. | 原溶液中有三种阳离子和两种阴离子 |
13.下列各种关于酸的使用,其中正确的是( )
| A. | 为了抑制Fe2+的水解,用稀硝酸酸化 | |
| B. | 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化 | |
| C. | 检验溶液中是否含有SO42-时,先用盐酸酸化 | |
| D. | 检验氯乙烷中的氯元素,水解后再用硫酸酸化 |
17.下列关于CO的叙述正确的是( )
| A. | CO的摩尔质量是28g | |
| B. | 1molCO的质量是28g/mol | |
| C. | 1molCO中所含分子数为6.02×1023个 | |
| D. | 常温常压下,1 molCO的体积为22.4 L |
7.已知:①2C(s)+O2(g)═2CO(g)△H=-220kJ•mol-1②氢气燃烧的能量变化示意图:
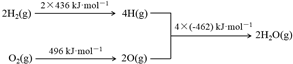
下列说法正确的是( )

下列说法正确的是( )
| A. | 1molC(s)完全燃烧放出110 kJ的热量 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-480 kJ•mol-1 | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H=+130 kJ•mol-1 | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ的热量 |
14.将0.1mol•L-1的KI溶液和0.05mol•L-1 Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-?2Fe2++I2”的是( )
| 实验编号 | 实验操作 | 实验现象 |
| ① | 滴入KSCN溶液 | 溶液变红色 |
| ② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
| ③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
| ④ | 滴入淀粉溶液 | 溶液变蓝色 |
| A. | ①和② | B. | ②和④ | C. | ③和④ | D. | ①和③ |
11.在某酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Mg2+、SO42-、HCO3- | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | Cu2+、Ca2+、Cl-、NO3- | D. | Fe2+、K+、NO3-、Cl- |
12.下列各组混合物中,用分液漏斗不能分离的是( )
| A. | 苯和水 | B. | 溴乙烷和水 | C. | 乙酸和乙醇 | D. | 乙酸乙酯和水 |