题目内容
如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法正确的是( )

| A、从E口逸出的气体是Cl2 |
| B、每生成22.4 LCl,便产生2 mol NaOH |
| C、从B口加入含少量NaOH的水溶液以增强导电性 |
| D、电解一段时间后加适量盐酸可以恢复到电解前的浓度 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据钠离子移动方向知,右边是阴极,左边是阳极,阴极上氢离子放电生成氢气,发生2H++2e-=H2↑,阳极上氯离子放电生成氯气,电极反应式为2Cl─-2e-=Cl2↑,电解时,阳极生成氯气,消耗NaCl,则应在阳极补充NaCl,阴极生成OH-,且Na+向阴极移动,则产品烧碱溶液从阴极区导出,据此分析.
解答:
解:A、右边是阴极区,发生2H++2e-=H2↑,所以从E口逸出的气体是H2,故A错误;
B、电池反应式为2NaCl+2H2O
Cl2↑+H2↑+2NaOH,标准状况下每生成22.4L Cl2,生成1mol氯气时,同时产生2molNaOH,因为温度和压强未知,无法计算氯气的物质的量,故B错误;
C、阴极生成OH-,且Na+向阴极移动,阴极区生成NaOH,为增强导电性,则从B口加入稀NaOH(增强导电性)的水溶液,故C正确;
D、电解生成氢气和氯气,电解一段时间后加适量HCl可以恢复到电解前的浓度,盐酸中有水,故D错误;
故选C.
B、电池反应式为2NaCl+2H2O
| ||
C、阴极生成OH-,且Na+向阴极移动,阴极区生成NaOH,为增强导电性,则从B口加入稀NaOH(增强导电性)的水溶液,故C正确;
D、电解生成氢气和氯气,电解一段时间后加适量HCl可以恢复到电解前的浓度,盐酸中有水,故D错误;
故选C.
点评:本题考查了电解原理,根据钠离子移动方向确定阴阳极,再结合电极上发生的反应来分析解答即可,注意阳离子交换膜只有阳离子才能通过,题目难度不大.

练习册系列答案
相关题目
下列离子方程式正确的是 ( )
| A、氯化铵与氢氧化钠两种溶液混合加热:NH4++OH-═NH3↑+H2O |
| B、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| C、氢氧化钠溶液中通入少量二氧化硫气体:SO2+OH-=HSO3- |
| D、氯化铝溶液中加入过量 氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
关于油和脂肪的下列说法正确的是( )
| A、二者互为同分异构体 |
| B、二者是同系物 |
| C、前者熔点低,后者熔点高 |
| D、在一定条件下前者可转化为后者 |
下列物质在水中最难电离的是( )
| A、CH3COOH |
| B、CH3CH2OH |
| C、H2O |
D、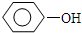 |
下列微粒半径大小比较不正确的是( )
| A、原子半径Na>Mg |
| B、原子半径F<S |
| C、离子半径Mg2+>O2- |
| D、离子半径Cl->Ca2+ |
下列反应的离子方程式书写正确的是( )
| A、饱和石灰水与稀硝酸反应:Ca(OH)2+2H+═Ca2++2H2O |
| B、稀硫酸与锌反应:H2SO4+Zn═Zn2++SO42++H2↑ |
| C、碳酸钙与稀硫酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| D、小苏打溶液与NaOH反应:HCO3-+OH-═H2O+CO32- |