题目内容
20.现有500mL物质的量浓度为1mol/L的NaOH溶液,与足量的铝完全反应,可消耗多少克铝?若产生标准状况下11.2L的H2,转移多少mol电子?分析 发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,n(NaOH)=0.5L×1mol/L=0.5mol,n(H2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,结合反应计算.
解答 解:n(NaOH)=0.5L×1mol/L=0.5mol,由2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,n(Al)=0.5mol,其质量为0.5mol×27g/mol=13.5g;
若产生标准状况下11.2L的H2,转移电子为0.5mol×2×(1-0)=1mol,
答:消耗Al为13.5g,若产生标准状况下11.2L的H2,转移1mol电子.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应或电子转移计算为解答的关键,侧重分析与计算能力的考查,注意利用化合价变化计算转移电子,题目难度不大.

练习册系列答案
相关题目
17.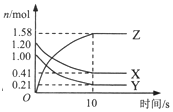 在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )
在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )
 在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )
在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )| A. | 反应开始到10s时,转化率:Y>X | |
| B. | 若前10s容器内的压强增加,说明生成Z的反应为放热反应 | |
| C. | 由图象可知前10s内生成Z的速率越来越快 | |
| D. | 若X为紫色,Y、Z无色,则10s后混合气体颜色不再变化 |
18.X、Y两种元素的原子最外层电子数分别为3和6,由X和Y组成的化合物其化学式可能是( )
| A. | X2Y | B. | X3Y2 | C. | X2Y3 | D. | Y3X2 |
8.某同学用某种粗盐进行提纯实验,步骤如图.
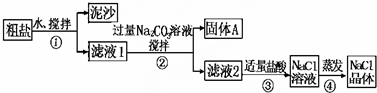
请回答:
(1)步骤①和②的操作相同,其名称是过滤.
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成固体(或溶液)飞溅,当蒸发皿中有较多量固体出现时,应停止加热(或熄灭酒精灯),用余热使水分蒸干.
(3)猜想和验证,补充完整相应的操作、现象和结论:

请回答:
(1)步骤①和②的操作相同,其名称是过滤.
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成固体(或溶液)飞溅,当蒸发皿中有较多量固体出现时,应停止加热(或熄灭酒精灯),用余热使水分蒸干.
(3)猜想和验证,补充完整相应的操作、现象和结论:
| 猜想 | 验证的操作 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含有BaCO3 | 取少量固体A于试管中,先滴入过量稀硝酸(或稀盐酸),再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 |
| 猜想Ⅱ:最后制得的NaCl晶体中还有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, 先滴入BaCl2溶液,再滴入过量稀HNO3 | 有白色沉淀 | 猜想Ⅱ成立 |
9.下列物质中互为同分异构体的是( )
| A. | 13C 与 14C | B. | CH3CH2OH与CH3COOH | ||
| C. | 甲烷与丙烷 | D. | CH3CH2CH2CH3 与 CH3CH(CH3)2 |
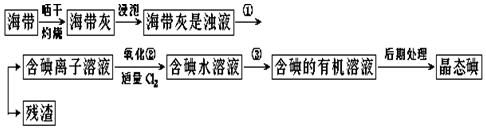
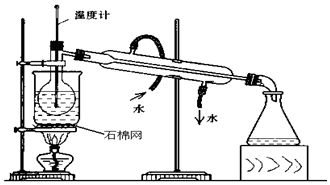
 欲设计一个实验验证红热的炭与浓硫酸发生反应所生成的各种产物.某同学设计的实验流程依次为:气体产物、无水硫酸铜、品红溶液1、酸性高锰酸钾、品红溶液2、澄清石灰水.
欲设计一个实验验证红热的炭与浓硫酸发生反应所生成的各种产物.某同学设计的实验流程依次为:气体产物、无水硫酸铜、品红溶液1、酸性高锰酸钾、品红溶液2、澄清石灰水.