题目内容
在下列各说法中,正确的是( )
| A、书写热化学方程式时任何反应条件都不能标注 |
| B、热化学方程式中的化学计量数表示物质的量,可以是分数 |
| C、任何酸与碱发生中和反应,生成1 mol H2O时放出的热量叫做中和热 |
| D、101KPa时,1 mol H2与在足量 O2中燃烧放出的热量就是H2的燃烧热 |
考点:热化学方程式,燃烧热,中和热
专题:化学反应中的能量变化
分析:A、温度压强不同,反应热不同,常温常压条件可以不标注,但其他条件需要标注;
B、热化学方程式中的化学计量数表示物质的量;
C、强酸强碱的稀溶液反应生成1mol水放出的热量为中和热,弱酸弱碱存在电离平衡,电离过程是吸热过程;
D、燃烧热是1mol可燃物完全反应生成稳定氧化物放出的热量;
B、热化学方程式中的化学计量数表示物质的量;
C、强酸强碱的稀溶液反应生成1mol水放出的热量为中和热,弱酸弱碱存在电离平衡,电离过程是吸热过程;
D、燃烧热是1mol可燃物完全反应生成稳定氧化物放出的热量;
解答:
解:A、温度压强不同,反应热不同,常温常压条件可以不标注,但其他条件需要标注,故A错误;
B、热化学方程式中的化学计量数表示物质的量,可以用分数表示,故B正确;
C、强酸强碱的稀溶液反应生成1mol水放出的热量为中和热,弱酸弱碱存在电离平衡,电离过程是吸热过程,所以任何酸与碱发生中和反应,生成1 mol H2O时放出的热量不全是中和热,故C错误;
D、燃烧热是1mol可燃物完全反应生成稳定氧化物放出的热量,101KPa时,1 mol H2与在足量 O2中燃烧生成液态水放出的热量就是H2的燃烧热,故D错误;
故选B.
B、热化学方程式中的化学计量数表示物质的量,可以用分数表示,故B正确;
C、强酸强碱的稀溶液反应生成1mol水放出的热量为中和热,弱酸弱碱存在电离平衡,电离过程是吸热过程,所以任何酸与碱发生中和反应,生成1 mol H2O时放出的热量不全是中和热,故C错误;
D、燃烧热是1mol可燃物完全反应生成稳定氧化物放出的热量,101KPa时,1 mol H2与在足量 O2中燃烧生成液态水放出的热量就是H2的燃烧热,故D错误;
故选B.
点评:本题考查了热化学方程式书写方法和表达意义,燃烧热、中和热概念实质理解,掌握实质是关键,题目较简单.

练习册系列答案
相关题目
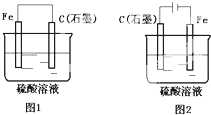 如图是化学能与电能相互转换的两套装置.对此两套装置的分析正确的是( )
如图是化学能与电能相互转换的两套装置.对此两套装置的分析正确的是( )| A、两装置中,铁电极上均有气体产生 |
| B、两装置中,石墨电极上均有气体产生 |
| C、石墨电极上发生的电极反应均为:2H++2e-=H2↑ |
| D、随着反应的进行,两装置中电解质溶液的酸性均减弱 |
设NA为阿伏加德罗常数的值.下列说法不正确的是( )
| A、常温常压下,13.8g NO2气体溶于足量水,转移电子数为0.2NA |
| B、标准状况下,22.41.CH3CI含有的原子数为5NA |
| C、0.5mo1O2与11.2LO2所含的分子数一定相等 |
| D、常温常压下,14g乙烯与丙烯的混合气体,含碳原子总数为NA |
下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B、25℃1.01×105Pa?64克SO2中含有的原子数为3NA |
| C、22.4LCH4与18gH2O所含有的电子数均为10NA |
| D、CO和N2分子含有的电子数相同,22.4L的CO气体与lmol N2所含的电子数相等 |
下列有机物命名正确的是( )
A、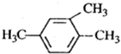 1,3,4-三甲苯 |
B、 2-氯丙烷 |
C、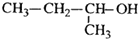 1-甲基-1-丙醇 |
D、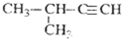 2-甲基-3-丁炔 |
2g AO32-中核外电子数比质子数多3.01×1022个,则元素A的摩尔质量是( )
| A、12g/mol |
| B、32g |
| C、80g/mol |
| D、32g/mol |

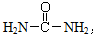 ,请写出尿素的同分异构体中含有离子键的化学式
,请写出尿素的同分异构体中含有离子键的化学式