题目内容
甲醇是一种优质的液体燃料,目前工业上CO和CO2均可用于合成甲醇.
(1)一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1;2CO(g)+O2(g)=2CO2(g)△H2;2H2(g)+O2(g)=2H2O(g)△H3;则CO(g)+2H2(g)?CH3OH(g)的△H= .
(2)在容积为2L的密闭容器中进行反应:
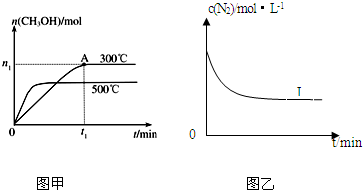
CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图甲.该反应的△H 0(填>、<或=).
(3)若要提高甲醇的产率,可采取的措施有 .(填字母)
A.缩小容器体积 B.降低温度
C.升高温度 D.使用合适的催化剂
E.甲醇从混合体系中分离出来
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,计算该温度下的平衡常数(写出计算过程,计算结果保留小数点后两位数字).
(5)工业上把水煤气中的混合气体处理后,获得较纯的H2用于Ⅰ合成氨:N2(g)+3H2(g)
2NH3(g)△H=-92.4kJ/mol某同学在不同实验条件下模拟化工生产进行实验,N2浓度随时间变化如图乙.实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在答题卷对应的地方画出实验I和实验Ⅲ中NH3浓度随时间变化的示意图.
(6)已知25℃KSP[Mg(OH)2]=1.8×10-11;KSP[Fe(OH)3]=2.6×10-39.在25℃下,向浓度均为0.1mol?L-1 MgCl2和FeCl3混合液中逐滴加入氨水,先生成沉淀(填化学式),生成沉淀的离子方程式为 .

(1)一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1;2CO(g)+O2(g)=2CO2(g)△H2;2H2(g)+O2(g)=2H2O(g)△H3;则CO(g)+2H2(g)?CH3OH(g)的△H=
(2)在容积为2L的密闭容器中进行反应:
CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图甲.该反应的△H
(3)若要提高甲醇的产率,可采取的措施有
A.缩小容器体积 B.降低温度
C.升高温度 D.使用合适的催化剂
E.甲醇从混合体系中分离出来
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,计算该温度下的平衡常数(写出计算过程,计算结果保留小数点后两位数字).
(5)工业上把水煤气中的混合气体处理后,获得较纯的H2用于Ⅰ合成氨:N2(g)+3H2(g)
| 一定条件 |
(6)已知25℃KSP[Mg(OH)2]=1.8×10-11;KSP[Fe(OH)3]=2.6×10-39.在25℃下,向浓度均为0.1mol?L-1 MgCl2和FeCl3混合液中逐滴加入氨水,先生成沉淀(填化学式),生成沉淀的离子方程式为
考点:用盖斯定律进行有关反应热的计算,化学平衡常数的含义,化学平衡的影响因素,物质的量或浓度随时间的变化曲线,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:(1)依据热化学方程式结合盖斯定律,计算所需热化学方程式,计量数改变,焓变改变,热化学方程式方向改变,焓变符号改变;
(2)图象分析,先拐先平,温度高,纵轴甲醇物质的量随温度升高减小,说明平衡逆向进行;
(3)若要提高甲醇的产率,平衡正向进行,结合平衡移动原理和反应特征分析,反应是气体体积减小的放热反应;
(4)依据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
(5)实验Ⅲ比实验Ⅰ的温度要高,达到平衡所需要时间短,反应是放热反应,升温平衡状态氨气的浓度减小;
(6)根据溶度积常数确定先沉淀的物质,溶度积常数越小的物质越先沉淀,铁离子和氨水反应生成氢氧化铁和铵根离子.
(2)图象分析,先拐先平,温度高,纵轴甲醇物质的量随温度升高减小,说明平衡逆向进行;
(3)若要提高甲醇的产率,平衡正向进行,结合平衡移动原理和反应特征分析,反应是气体体积减小的放热反应;
(4)依据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
(5)实验Ⅲ比实验Ⅰ的温度要高,达到平衡所需要时间短,反应是放热反应,升温平衡状态氨气的浓度减小;
(6)根据溶度积常数确定先沉淀的物质,溶度积常数越小的物质越先沉淀,铁离子和氨水反应生成氢氧化铁和铵根离子.
解答:
解:(1)①CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1;
②2CO(g)+O2(g)=2CO2(g)△H2;
③2H2(g)+O2(g)=2H2O(g)△H3;
依据盖斯定律①+
②-
③得到CO(g)+2H2(g)?CH3OH(g)的△H=△H1+
△H2-
△H3;
故答案为:△H1+
△H2-
△H3;
(2)图象分析,先拐先平,温度高,纵轴甲醇物质的量随温度升高减小,说明平衡逆向进行反应是放热反应,△H<0;
故答案为:<;
(3)CO(g)+2H2(g)?CH3OH(g),若要提高甲醇的产率,平衡正向进行,结合平衡移动原理和反应特征分析,反应是气体体积减小的放热反应;
A.缩小容器体积,压强增大,平衡正向进行,甲醇的产率增大,故A符合;
B.反应是放热反应,降低温度,平衡正向进行,甲醇的产率增大,故B符合;
C.反应是放热反应,升高温度,平衡逆向进行,甲醇产率减小,故C不符合;
D.使用合适的催化剂,只能改变化学反应速率不改变化学平衡状态,甲醇的产率不变,故D不符合;
E.甲醇从混合体系中分离出,减少生成物浓度,平衡正向进行,甲醇的产率增大,故E符合;
故答案为:ABE;
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,依据平衡三段式列式;
CH4 +H2O?CO+3H2
起始物质的量浓度(mol?L-1) 1.0 1.0 0 0
转化物质的量浓度(mol?L-1) 0.5 0.5 0.5 1.5
平衡物质的量浓度(mol?L-1 0.5 0.5 0.5 1.5
K=
=
=6.75mol2/L2;
答:该温度下的平衡常数6.75mol2/L2;
(5)实验Ⅲ比实验Ⅰ的温度要高,Ⅲ比Ⅰ快,达到平衡所需要时间短,反应是放热反应,升温平衡状态氨气的浓度减小,据此画出图象为:
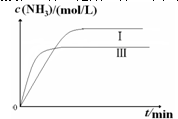
答:验I和实验Ⅲ中NH3浓度随时间变化的示意图为 ;
;
(6)溶度积常数越小的物质越先沉淀,氢氧化铁的溶度积小于氢氧化镁的溶度积,所以氢氧化铁先沉淀,铁离子和氨水反应生成氢氧化铁沉淀和铵根离子,离子方程式为Fe3++3NH3?H2O?Fe(OH)3↓+3NH4+;
故答案为:Fe(OH)3,Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
②2CO(g)+O2(g)=2CO2(g)△H2;
③2H2(g)+O2(g)=2H2O(g)△H3;
依据盖斯定律①+
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:△H1+
| 1 |
| 2 |
| 1 |
| 2 |
(2)图象分析,先拐先平,温度高,纵轴甲醇物质的量随温度升高减小,说明平衡逆向进行反应是放热反应,△H<0;
故答案为:<;
(3)CO(g)+2H2(g)?CH3OH(g),若要提高甲醇的产率,平衡正向进行,结合平衡移动原理和反应特征分析,反应是气体体积减小的放热反应;
A.缩小容器体积,压强增大,平衡正向进行,甲醇的产率增大,故A符合;
B.反应是放热反应,降低温度,平衡正向进行,甲醇的产率增大,故B符合;
C.反应是放热反应,升高温度,平衡逆向进行,甲醇产率减小,故C不符合;
D.使用合适的催化剂,只能改变化学反应速率不改变化学平衡状态,甲醇的产率不变,故D不符合;
E.甲醇从混合体系中分离出,减少生成物浓度,平衡正向进行,甲醇的产率增大,故E符合;
故答案为:ABE;
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,依据平衡三段式列式;
CH4 +H2O?CO+3H2
起始物质的量浓度(mol?L-1) 1.0 1.0 0 0
转化物质的量浓度(mol?L-1) 0.5 0.5 0.5 1.5
平衡物质的量浓度(mol?L-1 0.5 0.5 0.5 1.5
K=
| c3(H2)c(CO) |
| c(CH4)c(H2O) |
| 0.5mol/L×(1.5mol/L)3 |
| 0.5mol/L×0.5mol/L |
答:该温度下的平衡常数6.75mol2/L2;
(5)实验Ⅲ比实验Ⅰ的温度要高,Ⅲ比Ⅰ快,达到平衡所需要时间短,反应是放热反应,升温平衡状态氨气的浓度减小,据此画出图象为:

答:验I和实验Ⅲ中NH3浓度随时间变化的示意图为
 ;
;(6)溶度积常数越小的物质越先沉淀,氢氧化铁的溶度积小于氢氧化镁的溶度积,所以氢氧化铁先沉淀,铁离子和氨水反应生成氢氧化铁沉淀和铵根离子,离子方程式为Fe3++3NH3?H2O?Fe(OH)3↓+3NH4+;
故答案为:Fe(OH)3,Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
点评:本题考查了了热化学方程式和盖斯定律计算应用,图象分析、平衡影响因素理解应用、平衡常数计算、沉淀溶解平衡中溶度积的分析,主要是平衡移动原理的理解分析,图象分析方法是解题关键,题目难度中等.

练习册系列答案
相关题目
在日常生活中一次性使用聚乙烯用品会带来“白色污染”.这种材料难分解、难处理.聚乙烯的结构简式为  下列关于聚乙烯的说法错误的是( )
下列关于聚乙烯的说法错误的是( )
 下列关于聚乙烯的说法错误的是( )
下列关于聚乙烯的说法错误的是( )| A、由乙烯生成聚乙烯的反应属于加聚反应 |
| B、聚乙烯的单体为乙烯 |
| C、聚乙烯是一种纯净物 |
| D、聚乙烯结构简式中的n称为聚合度 |
NH3和纯净的O2在一定条件下发生反应:4NH3(g)+3O2(g)?2N2(g)+6H2O(g),现向一容积不变的2L密闭容器中充入4mol NH3和3mol O2,4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
| A、v(O2)=0.225mol?L-1?min-1 |
| B、v(H2O)=0.375mol?L-1?min-1 |
| C、v(N2)=0.125mol?L-1?min-1 |
| D、v(NH3)=0.250mol?L-1?min-1 |