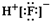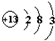题目内容
下列图式正确的是( )
分析:根据化学用语中的基本概念电子式、结构式、结构示意图、晶胞来进行解答.
A、HF为共价化合物,存在共用电子对;
B、次氯酸的结构式为H-O-Cl;
C、铝离子的质子数为13,核外电子数为10;
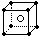
D、利用氯化铯与氯化钠都是体心立方晶体结构.
A、HF为共价化合物,存在共用电子对;
B、次氯酸的结构式为H-O-Cl;
C、铝离子的质子数为13,核外电子数为10;
D、利用氯化铯与氯化钠都是体心立方晶体结构.
解答:解:A、共价化合物电子式的书写是用.或x标出每个原子的最外层电子数以及原子间的共用电子对,使每个原子达到稳定结构,离子化合物电子式的书写是阴离子和复杂阳离子用[]括起来,在右上角标出电荷和电性,HF是共价化合物,不能写成离子化合物的形式,故A错误;
B、结构式的书写时原子的排列方式为:化合价绝对值大放中间,小的放周边,其结构式为H-O-Cl,故B错误;
C、考查的是原子结构示意图的书写,Al原子失去3个电子变成Al3+使次外层变成最外层,电子层由三层变为两层,最外层电子数为8,故C错误;
D、氯化铯晶胞是体心立方晶胞,配位数为8,故D正确.
故选D.
B、结构式的书写时原子的排列方式为:化合价绝对值大放中间,小的放周边,其结构式为H-O-Cl,故B错误;
C、考查的是原子结构示意图的书写,Al原子失去3个电子变成Al3+使次外层变成最外层,电子层由三层变为两层,最外层电子数为8,故C错误;
D、氯化铯晶胞是体心立方晶胞,配位数为8,故D正确.
故选D.
点评:本题考查的是化学用语,具有综合性,属于基础题,本题中的B是学生解答的易错点,D是学生解答的难点,学生应学会利用类比的方法来解答.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列叙述与对应图式正确的是( )

A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
| |||||||||||||||||||||||||||
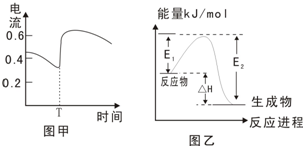
| B、图甲表示Zn-Cu原电池反应过程中的电流强度的变化.T时可能加入了H2O2 | |||||||||||||||||||||||||||
| C、图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 | |||||||||||||||||||||||||||
| D、图丙表示元素周期表的一部分,元素X,Y,Z、W中X的氢化物酸性最强 |
下列叙述与对应图式正确的是( )
 |
下列叙述与对应图式正确的是
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径最高或最低化合价 | 0.74 | 1.60 +2 | 1.52 +1 | 1.10 +5 | 0.99 +7 | 1.86 +1 | 0.75 +5 | 0.82 +3 |
—2 | —3 | —1 | —3 |
A
.由下列短周期元素性质的数据推断元素最高价氧化物对应的水化物碱性最强
B.图甲表示Zn—Cu原电池反应过程中的电流强度的变化。T时可能加入了H2O2
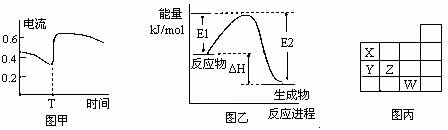
C.图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变
D.图丙表示元素周期表的一部分,元素X,Y,Z、W中X的氢化物酸性最强