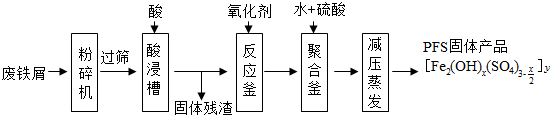
题目内容
6.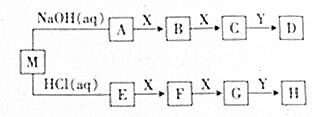 几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.
几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.回答下列问题:
(1)M的化学式为NH4HS;A的电子式为
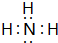 .
.(2)写出在M中滴加盐酸的离子方程式:HS-+H+=H2S↑.
(3)写出A生成B的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(4)G在加热条件下与白磷(P4)反应生成两种氧化物,写出该反应的化学方程式:10SO3+P4$\frac{\underline{\;\;△\;\;}}{\;}$10SO2+2P2O5.
分析 中学常见的短周期元素组成几种物质,X是单质,B、C、F、G、Y都是氧化物,B与X反应生成C,E与X连续反应生成G,可知X为O2,D和H是两种常用的强酸,由转化关系可知D为HNO3、H为H2SO4,Y为H2O,则A为NH3,B为NO,C为NO2,E为H2S,F为SO2,G为SO3,M是酸式盐,则M为NH4HS.
解答 解:中学常见的短周期元素组成几种物质,X是单质,B、C、F、G、Y都是氧化物,B与X反应生成C,E与X连续反应生成G,可知X为O2,D和H是两种常用的强酸,由转化关系可知D为HNO3、H为H2SO4,Y为H2O,则A为NH3,B为NO,C为NO2,E为H2S,F为SO2,G为SO3,M是酸式盐,则M为NH4HS.
(1)M的化学式为NH4HS,A为NH3,电子式为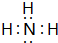 ,
,
故答案为:NH4HS;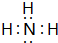 ;
;
(2)在M中滴加盐酸的离子方程式:HS-+H+=H2S↑,
故答案为:HS-+H+=H2S↑;
(3)A生成B的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)G在加热条件下与白磷(P4)反应生成两种氧化物,该反应的化学方程式为:10SO3+P4$\frac{\underline{\;\;△\;\;}}{\;}$10SO2+2P2O5,
故答案为:10SO3+P4$\frac{\underline{\;\;△\;\;}}{\;}$10SO2+2P2O5.
点评 本题考查无机物推断,涉及N、S元素单质化合物性质,转化中连续反应及D、H为中学常见强酸是推断突破口,熟练掌握元素化合物知识,识记中学常见的连续反应.

练习册系列答案
相关题目
16.短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示.下列说法一定正确的是( )


| A. | 最高正化合价:Z>X | |
| B. | X、Y、Z的单质中,Z单质的熔点最高 | |
| C. | 若X为非金属元素,则离子半径:Xn->Ym->Zm- | |
| D. | X最高价氧化物对应的水化物,要么是强酸,要么是强碱 |
17.在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体[(NH4)2S4•FeSO4•6H2O],该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
(1)配制FeSO4溶液时需要加入少量稀硫酸的目的是抑制FeSO4的水解,判断FeSO4溶液是否变质的方法是取适量FeSO4溶液于试管中,向溶液中加入KSCN溶液,若溶液变红,则说明FeSO4溶液变质,无现象则不变质.
(2)实验室通常向FeSO4溶液中加入饱和(NH4)2SO4溶液,然后经过“一系列操作”后得到硫酸亚铁铵晶体,其中“一系列操作”依次为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)为了洗涤硫酸亚铁铵晶体的粗产品,下列方法中最合适的是d(填字母).
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用Na2SO4熔液洗 d.用无水乙醇洗
(4)为了测定硫酸亚铁晶体产品的纯度,称取ag产品溶于水,配制成500mL溶液,取待测液25.00mL
用浓度为cmol•L-1的酸性KMnO4溶液滴定.重复上述操作2次,实验结果如下:
①滴定过程中发生反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O.
②滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色,.
③该产品的纯度为$\frac{980c}{a}$×100%(用含a、c的代数式表示).
④上表中第一次实验记录的数据明显大于后两次,其原因可能是bc(填字母).
a.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
b.滴定前滴定管尖嘴有气泡,滴定结束无气泡
c.第一次滴定用的锥形瓶用待装液润洗过,后两次来润洗
d.该酸性高锰酸钾标准液未用硫酸酸化,改用硝酸酸化.
(1)配制FeSO4溶液时需要加入少量稀硫酸的目的是抑制FeSO4的水解,判断FeSO4溶液是否变质的方法是取适量FeSO4溶液于试管中,向溶液中加入KSCN溶液,若溶液变红,则说明FeSO4溶液变质,无现象则不变质.
(2)实验室通常向FeSO4溶液中加入饱和(NH4)2SO4溶液,然后经过“一系列操作”后得到硫酸亚铁铵晶体,其中“一系列操作”依次为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)为了洗涤硫酸亚铁铵晶体的粗产品,下列方法中最合适的是d(填字母).
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用Na2SO4熔液洗 d.用无水乙醇洗
(4)为了测定硫酸亚铁晶体产品的纯度,称取ag产品溶于水,配制成500mL溶液,取待测液25.00mL
用浓度为cmol•L-1的酸性KMnO4溶液滴定.重复上述操作2次,实验结果如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液的体积/ml | 25.52 | 25.02 | 24.98 |
②滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色,.
③该产品的纯度为$\frac{980c}{a}$×100%(用含a、c的代数式表示).
④上表中第一次实验记录的数据明显大于后两次,其原因可能是bc(填字母).
a.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
b.滴定前滴定管尖嘴有气泡,滴定结束无气泡
c.第一次滴定用的锥形瓶用待装液润洗过,后两次来润洗
d.该酸性高锰酸钾标准液未用硫酸酸化,改用硝酸酸化.
14.以下事实中可以用相似相溶原理说明的是( )
| A. | HCl易溶于水 | B. | I2可溶于水 | C. | Cl2可溶于水 | D. | CO2可溶于水 |
1. 短周期元素A、B、C、D的原子序数依次增大,它们在元素周期表中的相对位置如图所示,已知C和A的原子序数之差等于A的原子序数,下列说法正确的是( )
短周期元素A、B、C、D的原子序数依次增大,它们在元素周期表中的相对位置如图所示,已知C和A的原子序数之差等于A的原子序数,下列说法正确的是( )
 短周期元素A、B、C、D的原子序数依次增大,它们在元素周期表中的相对位置如图所示,已知C和A的原子序数之差等于A的原子序数,下列说法正确的是( )
短周期元素A、B、C、D的原子序数依次增大,它们在元素周期表中的相对位置如图所示,已知C和A的原子序数之差等于A的原子序数,下列说法正确的是( )| A. | 原子半径:D>C>B>A | |
| B. | 简单离子半径:D>A>B | |
| C. | 简单氢化物的稳定性:D>C>A | |
| D. | 四种元素的最高价氧化物均可溶于水 |
11.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解:再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,震荡后仍有固体存在.
该白色粉末可能为( )
①取少量样品加入足量水仍有部分固体未溶解:再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,震荡后仍有固体存在.
该白色粉末可能为( )
| A. | NaHCO3、Al(OH)3 | B. | AgCl、NaHCO3 | C. | Na2SO3、BaCO3 | D. | Na2CO3、CuSO4 |
18. 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1r溶液的pH为2,s通常是难溶于水的混合物.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1r溶液的pH为2,s通常是难溶于水的混合物.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1r溶液的pH为2,s通常是难溶于水的混合物.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1r溶液的pH为2,s通常是难溶于水的混合物.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小W<X<Y | B. | 元素的非金属性Z>X>Y | ||
| C. | Y的氢化物常温常压下为液态 | D. | X的最高价氧化物的水化物为强酸 |
1.仅能在水溶液中导电的电解质是( )
| A. | KOH | B. | KNO3 | C. | NH4HCO3 | D. | 酒精 |