题目内容
3.在15g铁和氧化铁的混合物中加入150mL稀H2SO4放出氢气1.68L(标准状况).当反应停止后,铁和氧化铁均无剩余,且溶液中无Fe3+存在.为了中和过量H2SO4,并使Fe2+完全转化为Fe(OH)2沉淀,共耗用3mol/L NaOH溶液200mL.求:(1)混合物中铁的质量为7g
(2)稀H2SO4的物质的量浓度为2mol•L-1.
分析 (1)铁和氧化铁均无剩余,且溶液中无Fe3+存在,反应生成FeSO4,设Fe、氧化铁的物质的量分别为xmol、ymol,根据二者质量及电子转移守恒列方程计算解答;
(2)铁和氧化铁与硫酸反应后溶液中溶质为FeSO4、H2SO4,加入NaOH使Fe2+完全转化为Fe(OH)2沉淀,产生反应后的溶液溶质只有Na2SO4,根据硫酸根守恒则n(H2SO4)=n(Na2SO4),根据钠离子守恒则n(Na2SO4)=$\frac{1}{2}$n(NaOH),进而计算硫酸的物质的量浓度.
解答 解:(1)铁和氧化铁与硫酸反应均无剩余,且溶液中无Fe3+存在,反应生成FeSO4,生成氢气为$\frac{1.68L}{22.4L/mol}$=0.075mol,
设Fe、氧化铁的物质的量分别为xmol、ymol,则:
根据二者质量,可得:56x+160y=15
根据电子转移守恒,可得:2x=2y+0.075×2
联立方程,解得x=0.125,y=0.05
故m(Fe)=0.125mol×56g/mol=7g,
故答案为:7;
(2)铁和氧化铁与硫酸反应后溶液中溶质为FeSO4、H2SO4,加入NaOH使Fe2+完全转化为Fe(OH)2沉淀,产生反应后的溶液溶质只有Na2SO4,根据硫酸根守恒则n(H2SO4)=n(Na2SO4),根据钠离子守恒则n(Na2SO4)=$\frac{1}{2}$n(NaOH)=$\frac{1}{2}$×3mol/L×0.2L=0.3mol,c(H2SO4)=$\frac{0.3mol}{0.15L}$=2mol/L,
故答案为:2.
点评 本题考查混合物计算,清楚发生的反应是解题关键,注意利用守恒思想计算,侧重学生分析计算能力的考查,难度中等.

练习册系列答案
相关题目
14.下列反应中,属于氧化反应的是( )
| A. | 乙烷在光照下与氯气反应 | B. | 乙烯使酸性高锰酸钾溶液褪色 | ||
| C. | 乙烯使溴水褪色 | D. | 苯与液溴混合后撒入铁粉 |
11.下列有关氯气及其化合物的说法不正确的是( )
| A. | 因为氯气有毒,有强氧化性,所以可用于杀菌、消毒、漂白 | |
| B. | 干燥的氯气和氯水均能使鲜花褪色 | |
| C. | 除去氯气中少量氯化氢可使气体通过饱和食盐水 | |
| D. | 氯气能与大多数金属化合,其一般将变价金属氧化至最高价 |
18.下列有关实验的叙述正确的是( )
| A. | 用苯萃取碘水中的碘时,将碘的苯溶液从分液漏斗下口放出 | |
| B. | Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | |
| C. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| D. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
12.光纤通讯已经成为信息化社会必不可少的高科技通讯手段.下列物质用于制造光纤通讯材料的是( )
| A. | 金刚石 | B. | 焦炭 | C. | 大理石 | D. | 石英 |
13.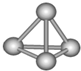 最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
 最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )| A. | N4属于一种新型的化合物 | |
| B. | N4与N2互称为同位素 | |
| C. | N4化学性质比N2稳定 | |
| D. | 1molN4沸气体转变为N2将放出882kJ热量 |