题目内容
一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g.甲烷的质量为( )
| A、12.5g |
| B、13.2g |
| C、11.2g |
| D、24.4g |
考点:化学方程式的有关计算
专题:计算题
分析:CH4燃烧产物为CO、CO2、H2O(g),产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,根据n=
可以计算出水的物质的量,再根据H原子守恒可计算CH4的物质的量及质量.
| m |
| M |
解答:
解:当其缓缓通过无水CaCl2时CaCl2增重25.2克,即气体质量减少25.2g,减少的气体为水蒸气,
则水的质量为25.2g,水的物质的量为:n(H2O)=
=1.4mol,
1.4mol水中含有H原子的物质的量为:n(H)=1.4mol×2=2.8mol,
根据H原子守恒可知,甲烷的物质的量为:n(CH4)=
=
=0.7mol,
所以甲烷的质量为:m(CH4)=16g/mol×0.7mol=11.2g,
故选C.
则水的质量为25.2g,水的物质的量为:n(H2O)=
| 25.2g |
| 18g/mol |
1.4mol水中含有H原子的物质的量为:n(H)=1.4mol×2=2.8mol,
根据H原子守恒可知,甲烷的物质的量为:n(CH4)=
| n(H) |
| 4 |
| 2.8mol |
| 4 |
所以甲烷的质量为:m(CH4)=16g/mol×0.7mol=11.2g,
故选C.
点评:本题考查有机物燃烧反应的计算,题目难度不大,注意掌握根据化学方程式进行的化学计算方法,解题关键是抓住化学反应前后H原子守恒守恒.

练习册系列答案
相关题目
下列说法正确的是( )
| A、NaOH溶于水共价键被破坏 |
| B、稀有气体的原子间存在共价键 |
| C、二氧化碳分子的结构式:O═C═O |
| D、MgF2、H2O2含有的化学键类型相同 |
分离苯和苯酚的混合物,通常采用的方法是( )
| A、振荡混合物,用分液漏斗分离 |
| B、加水振荡后,用分液漏斗分离 |
| C、加稀盐酸振荡后,用分液漏斗分离 |
| D、加入NaOH溶液后振荡,用分液漏斗分离,取下层液体通入CO2,待分层后分离 |
 含一个碳碳三键的炔烃加氢后的结构简式为该炔烃可能的结构有( )
含一个碳碳三键的炔烃加氢后的结构简式为该炔烃可能的结构有( )| A、2种 | B、3种 | C、4种 | D、5种 |
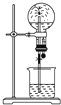 喷泉是一种常见的自然现象,如图是化学教材中常用的喷泉实验装置(夹持仪器已略去),在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体;下列气体和液体的组合中不可能形成喷泉的是( )
喷泉是一种常见的自然现象,如图是化学教材中常用的喷泉实验装置(夹持仪器已略去),在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体;下列气体和液体的组合中不可能形成喷泉的是( )| A、HCl和H2O |
| B、O2和H2O |
| C、NH3和H2O |
| D、CO2和NaOH溶液 |
往下列溶液中滴加FeCl3溶液,无变化的是( )
A、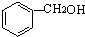 |
B、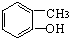 |
C、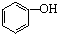 |
| D、氢碘酸 |
下列有关实验中叙述不正确的是( )
| A、向2mL 5% H2O2溶液中滴入0.1 mol/L FeCl3溶液1 mL,能较快的产生气体 |
| B、向KMnO4酸性溶液中加入过量草酸溶液,溶液紫红色褪去 |
| C、向酸性K2Cr2O7溶液中加入适量的NaOH溶液,溶液由黄色变为橙色 |
| D、向5mL 0.1mol/L Na2S2O3溶液中加入稀H2SO4,一段时间后溶液变浑浊 |
下列各组溶液中,因氧化还原反应不能大量共存的离子组是( )
| A、Na+、HCO3-、Cl- |
| B、Cu2+、Na+、SO42- |
| C、K+、SO42-、OH- |
| D、Fe2+、Al3+、NO3-、H+ |