题目内容
已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
A.该溶液的c(H+) = 10-4 mol/L
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.将此溶液加水稀释后,电离的HA分子数大于0.1%
B
【解析】
试题分析:A、该溶液中的氢离子浓度为0.1×0.1%= 10-4 mol/L ,故正确,不选A;B、升高温度,平衡正向移动,氢离子浓度增大,pH减小,故选B;C、根据电离平衡常数的计算公式,电离平衡常数=(0.1×0.1%)(0.1×0.1%)÷0.1=1×10-7,故正确,不选C;D、加水稀释后,电离平衡正向移动,电离的分子比原来多,故正确,不选D、
考点:弱电解质的电离。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(19分)(1)已知拆开1 mol H—H键、1 mol I—I、1 mol H—I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ,则由氢气和碘反应生成1 mol HI需要 (填“放出”或“吸收”) kJ的热量。
(2)已知在常温常压下:
①CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H1=-442.8 kJ/mol
②2CO(g)+O2(g)=2CO2(g);ΔH2 =-566.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式__________________________________________
(3)已知合成氨的热化学方程式为:N2(g)+3H2(g) 2NH3(g);ΔH= -92.2 kJ·mol-1
2NH3(g);ΔH= -92.2 kJ·mol-1
下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为 kJ。
②0~1小时内N2的平均反应速率 mol·L-1·h-1
③此条件下该反应的化学平衡常数K= (保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1mol,化学平衡向 方向移动(填“正反应”或“逆反应”或“不移动”)
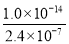 mol·L-1 D.无法确定
mol·L-1 D.无法确定 时间(h)
时间(h)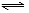 2HI(g)达到平衡的标志是
2HI(g)达到平衡的标志是 2Fe+3CO2的下列说法中正确的是
2Fe+3CO2的下列说法中正确的是 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则