题目内容
用1~18号元素及其形成的化合物按要求填空.
(1)除稀有气体外,原子半径最小的元素是 ,原子半径最大的元素是 ,其形成的离子结构示意图是 .
(2)用电子式表示金属性最强的元素和非金属性最强的元素组成的化合物的形成过程 .
(3)最高价氧化物的水化物碱性最强的是 ,最高价氧化物的水化物酸性最强的是 ,最高价氧化物的水化物为两性氢氧化物的是 ,以上三种物质两两之间反应的离子方程式为 , , .
(4)某元素气态氢化物的水溶液呈碱性,写出该氢化物的电子式 .
(1)除稀有气体外,原子半径最小的元素是
(2)用电子式表示金属性最强的元素和非金属性最强的元素组成的化合物的形成过程
(3)最高价氧化物的水化物碱性最强的是
(4)某元素气态氢化物的水溶液呈碱性,写出该氢化物的电子式
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)原子的电子层数越少,其原子半径越小,同一周期元素中,原子半径随着原子序数增大而减小;
(2)金属性最强的元素是Na元素、非金属性最强的元素是F元素,二者形成的化合物是NaF,Na原子和F原子通过得失电子形成离子化合物NaF;
(3)元素的金属性越强,其最高价氧化物的水化物碱性越强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,最高价氧化物的水化物为两性氢氧化物的是氢氧化铝,三种物质两两之间能发生反应;
(4)气态氢化物的水溶液呈碱性的气体是NH3,氨气分子中N原子和每个H原子共用一对电子.
(2)金属性最强的元素是Na元素、非金属性最强的元素是F元素,二者形成的化合物是NaF,Na原子和F原子通过得失电子形成离子化合物NaF;
(3)元素的金属性越强,其最高价氧化物的水化物碱性越强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,最高价氧化物的水化物为两性氢氧化物的是氢氧化铝,三种物质两两之间能发生反应;
(4)气态氢化物的水溶液呈碱性的气体是NH3,氨气分子中N原子和每个H原子共用一对电子.
解答:
解:(1)原子的电子层数越少,其原子半径越小,同一周期元素中,原子半径随着原子序数增大而减小,原子半径最小的是H元素、最大的是Na元素,钠离子结构示意图为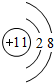 ,故答案为:H;Na;
,故答案为:H;Na;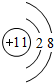 ;
;
(2)金属性最强的元素是Na元素、非金属性最强的元素是F元素,二者形成的化合物是NaF,其形成过程为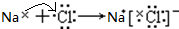 ,故答案为:
,故答案为: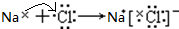 ;
;
(3)Na的金属性最强,则NaOH的碱性最强,F元素的非金属性最强,但F元素没有最高价氧化物的水化物,最高价氧化物的水化物酸性最强的是HClO4,最高价氧化物的水化物为两性氢氧化物的是Al(OH)3,三种物质两两之间离子反应方程式为分别为H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:NaOH;HClO4;Al(OH)3;H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O;
(4)气态氢化物的水溶液呈碱性的气体是NH3,其电子式为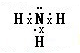 ,故答案为:
,故答案为: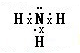 .
.
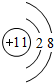 ,故答案为:H;Na;
,故答案为:H;Na;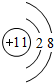 ;
;(2)金属性最强的元素是Na元素、非金属性最强的元素是F元素,二者形成的化合物是NaF,其形成过程为
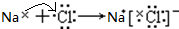 ,故答案为:
,故答案为: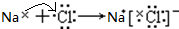 ;
;(3)Na的金属性最强,则NaOH的碱性最强,F元素的非金属性最强,但F元素没有最高价氧化物的水化物,最高价氧化物的水化物酸性最强的是HClO4,最高价氧化物的水化物为两性氢氧化物的是Al(OH)3,三种物质两两之间离子反应方程式为分别为H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:NaOH;HClO4;Al(OH)3;H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O;
(4)气态氢化物的水溶液呈碱性的气体是NH3,其电子式为
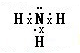 ,故答案为:
,故答案为: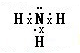 .
.
点评:本题考查了元素周期表及元素周期律综合应用,涉及电子式、离子方程式、原子结构等化学用语,再结合元素周期律分析解答,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、25℃,NaHCO3在水中的溶解度比Na2CO3的小 |
| B、Na2O和Na2O2中的阴阳离子个数比不相等 |
| C、用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色说明原溶液中有Na+无K+ |
| D、Na与足量O2反应,随温度升高生成Na2O的速率逐渐加快 |
常温下,下列溶液中酸性最弱的是( )
| A、pH=4 |
| B、[H+]=1×10-3mol?L-1 |
| C、[OH-]=1×10-12mol?L-1 |
| D、[OH-]=1×10-14mol?L-1 |
在酸性溶液中能大量共存的溶液是( )
| A、K+、Cl-、Al3+、SO42- |
| B、Na+、NH4+、NO3-、CO32- |
| C、Fe2+、NO3-、SO42-、Mg2+ |
| D、Na+、SO42-、K+、OH- |
下列离子方程式正确的是( )
| A、澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、钠与水反应:Na+2H2O=Na++OH-+H2↑ |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、铝片放入氢氧化钠溶液中:2Al+2H2O+2OH-=2AlO2-+3H2↑ |
 A、B两种固体物质的溶解度曲线如图所示.请回答:
A、B两种固体物质的溶解度曲线如图所示.请回答: