题目内容
下列叙述正确的是( )
| A、1molNaOH的质量为40g?mol-1 |
| B、标准状况下,1molH2O2的体积为22.4L |
| C、3.01×1023个SO2分子的质量为32g |
| D、CH4的摩尔质量为16g |
考点:摩尔质量,气体摩尔体积
专题:化学用语专题
分析:A.根据质量的单位判断;
B.Vm=22.4L/mol用于标准状况下的气体;
C.根据n=
=
计算;
D.根据摩尔质量的单位判断.
B.Vm=22.4L/mol用于标准状况下的气体;
C.根据n=
| m |
| M |
| N |
| NA |
D.根据摩尔质量的单位判断.
解答:
解:A.质量的单位是g,故A错误;
B.1molH2O2的体积不是22.4L,标准状况下过氧化氢为液体,故B错误;
C.n(SO2)=
=0.5mol,m(SO2)=0.5mol×64g/mol=32g,故C正确;
D.摩尔质量的单位为g/mol,故D错误;
故选C.
B.1molH2O2的体积不是22.4L,标准状况下过氧化氢为液体,故B错误;
C.n(SO2)=
| 3.01×1023 |
| 6.02×1023/mol |
D.摩尔质量的单位为g/mol,故D错误;
故选C.
点评:本题考查了摩尔质量、阿伏伽德罗常数及其相关计算,难度不大,注意各自的单位.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1 H2(g)+O2(g)═H2O(l)△H=-285.8kJ?mol-1由此可知,在等温下蒸发36g液态水需吸收的热量( )
| A、483.6 kJ |
| B、88 kJ |
| C、285.8 kJ |
| D、44 kJ |
下列化学用语正确的是( )
| A、氯化钙的化学式 CaCl |
B、镁离子结构示意图: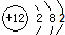 |
| C、碳酸钠的电离方程式 Na2CO3=Na++CO32- |
| D、氢氧化钡的电离方程式Ba(OH)2=Ba2++2OH- |
下列叙述正确的是( )
| A、1.00 mol NaCl中含有6.02×1023个NaCl分子 |
| B、1.00 mol NaCl中,所有Na+的最外层电子总数为10×6.02×1023 |
| C、欲配置1.00L、1.00 mol.L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| D、1mol Fe与稀硫酸反应Fe失去的电子数为2NA |
下列有关摩尔使用的说法中不正确的是( )
| A、1mol O |
| B、1mol O2 |
| C、1mol氧分子 |
| D、1摩尔苹果 |
下列叙述正确的是( )
| A、相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 |
| B、等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等 |
| C、常温常压下28 g CO与22.4 L O2所含分子数相等 |
| D、16 g CH4与18 g NH所含质子数相等 |
下列文字表述与反应方程式对应且正确的是( )
| A、溴乙烷中滴入硝酸银溶液检验其中的溴元素:Ag++Br-=AgBr↓ | ||||
| B、14g乙烯燃烧生成液态水产生b kJ热量,则表示其燃烧热的热化学方程式为:C2H4(g)+3 O2(g)═2 H2O(g)+2 CO2(g)△H=-2 b kJ?mol-1 | ||||
C、用惰性电极电解饱和KCl溶液:2 H++2 Cl-
| ||||
| D、硫酸亚铁与双氧水、稀H2SO4混合:2 Fe2++H2O2+2 H+=2 Fe3++2 H2O |