题目内容
 铁及铁化合物在生产、生活中有着重要的用途.
铁及铁化合物在生产、生活中有着重要的用途.(1)已知铁是26号元素,写出Fe的价层电子电子排布式
(2)Fe原子或离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物,则与之形成配合物的分子的配位原子应具备的结构特征是
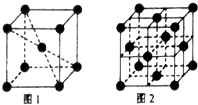
(3)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,在两种晶体中最邻近的铁原子间距离相同.
①图1和图2中,铁原子的配位数之比为
②空间利用率是指构成晶体的原子、离子或分子在整个晶体空间中占有的体积百分比,则图1和图2中,铁原子的空间利用率之比为
考点:晶胞的计算,原子核外电子排布,“等电子原理”的应用
专题:化学键与晶体结构
分析:(1)根据核外电子排布规律书写该元素原子的价电子排布式;根据质子数和中子数计算出质量数,写出同位素符号;
(2)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;根据等电子体原理可以写出一氧化碳的等电子体;根据分子的极性对物质性质的影响作判断;
(3)①1183K以下,与位于顶点的铁原子等距离且最近的铁原子位于晶胞体心,顶点的铁原子被8个晶胞共有,以此判断配位数;1183K以上,与铁原子等距离且最近的铁原子位于面心,则距离顶点的铁原子距离且最近的铁原子,横平面有4个、竖平面有4个、平行于纸面的有4个,共12个,以此判断配位数之比;
②设晶胞边长为a,原子半径为r,根据晶胞结构图可知,图1为体心立方结构,3a2=(4r)2,得r=
a,其空间利用率为
×100%=
×100%=68%,而图2为面心立方结构,2a2=(4r)2,得r=
a,其空间利用率为
×100%=
×100%=74%,据此可以算出空间利用率之比;
(2)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;根据等电子体原理可以写出一氧化碳的等电子体;根据分子的极性对物质性质的影响作判断;
(3)①1183K以下,与位于顶点的铁原子等距离且最近的铁原子位于晶胞体心,顶点的铁原子被8个晶胞共有,以此判断配位数;1183K以上,与铁原子等距离且最近的铁原子位于面心,则距离顶点的铁原子距离且最近的铁原子,横平面有4个、竖平面有4个、平行于纸面的有4个,共12个,以此判断配位数之比;
②设晶胞边长为a,原子半径为r,根据晶胞结构图可知,图1为体心立方结构,3a2=(4r)2,得r=
| ||
| 4 |
| 晶胞所含原子体积 |
| 晶胞体积 |
2×
| ||
| a3 |
| ||
| 4 |
| 晶胞所含原子体积 |
| 晶胞体积 |
4×
| ||
| a3 |
解答:
解:(1)该元素的原子序数是26,核外电子数为26,该元素原子的电子排布式为1s22s22p63s23p63d64s2,价电子排布式为d64s2,中子数为30的铁原子的质量数为30+26=56,所以该种同位素符号为5626Fe,故答案为:3d64s2;5626Fe;
(2)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;价电子数和原子数都分别相等的微粒称为等电子体,所以CO的等电子体是N2,结构式为N≡N;由于CO为极性分子,而氮气是非极性分子,所以CO的沸点高于氮气,故答案为:具有孤对电子;N≡N;CO;
(3)①1183K以下,与位于顶点的铁原子等距离且最近的铁原子位于晶胞体心,顶点的铁原子被8个晶胞共有,则配位数为8;1183K以上,与铁原子等距离且最近的铁原子位于面心,则距离顶点的铁原子距离且最近的铁原子,横平面有4个、竖平面有4个、平行于纸面的有4个,共12个,配位数之比为2:3,故答案为:2:3;
②设晶胞边长为a,原子半径为r,根据晶胞结构图可知,图1为体心立方结构,3a2=(4r)2,得r=
a,其空间利用率为
×100%=
×100%=68%,而图2为面心立方结构,2a2=(4r)2,得r=
a,其空间利用率为
×100%=
×100%=74%,所以它们的利用率之比为68:74=0.92:1,故答案为:0.92:1;
(2)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;价电子数和原子数都分别相等的微粒称为等电子体,所以CO的等电子体是N2,结构式为N≡N;由于CO为极性分子,而氮气是非极性分子,所以CO的沸点高于氮气,故答案为:具有孤对电子;N≡N;CO;
(3)①1183K以下,与位于顶点的铁原子等距离且最近的铁原子位于晶胞体心,顶点的铁原子被8个晶胞共有,则配位数为8;1183K以上,与铁原子等距离且最近的铁原子位于面心,则距离顶点的铁原子距离且最近的铁原子,横平面有4个、竖平面有4个、平行于纸面的有4个,共12个,配位数之比为2:3,故答案为:2:3;
②设晶胞边长为a,原子半径为r,根据晶胞结构图可知,图1为体心立方结构,3a2=(4r)2,得r=
| ||
| 4 |
| 晶胞所含原子体积 |
| 晶胞体积 |
2×
| ||
| a3 |
| ||
| 4 |
| 晶胞所含原子体积 |
| 晶胞体积 |
4×
| ||
| a3 |
点评:本题主要考查了价电子排布式、配合物的结构、金属晶体的结构,中等难度,解题时要注意基础知识的运用,要熟记常见晶胞的结构和空间利用率.

练习册系列答案
相关题目
下列关于胶体的叙述中,正确的是( )
| A、胶体是一种分散质直径小于10-10m的分散系 |
| B、胶体一定是液态的 |
| C、用一束光线照射胶体,在垂直于光线的方向可看到一条光亮的通路 |
| D、蛋白质溶液不是一种胶体 |
 某小组通过对人呼吸中各种气体体积分数的实验探究,得到下表所示数据:
某小组通过对人呼吸中各种气体体积分数的实验探究,得到下表所示数据: