题目内容
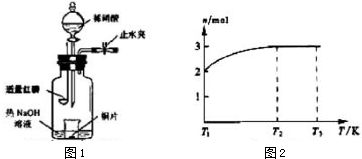
3.二氧化氮能形成二聚分子:2NO2(g)?N2O4(g)正反应放热,现欲测定NO2分子的相对质量,应采取的措施是( )| A. | 高温、低压 | B. | 低温、高压 | C. | 低温、低压 | D. | 高温、高压 |
分析 2NO2(g)?N2O4(g)为体积减小、且正反应放热的反应,欲测定NO2分子的相对质量,应使平衡逆向移动,以此来解答.
解答 解:2NO2(g)?N2O4(g)为体积减小、且正反应放热的反应,则减小压强平衡逆向移动、升高温度平衡逆向移动,则欲测定NO2分子的相对质量,应采取的措施是高温、低压,
故选A.
点评 本题考查化学平衡的移动,为高频考点,把握化学反应的特点、温度和压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意测定NO2分子的相对质量与平衡移动的关系,题目难度不大.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
12.下列有关说法正确的是( )
| A. | 目前我国流通的硬币是由合金材料制成的 | |
| B. | Al与S直接化合可以得到Al2S3,则Fe与S直接化合也可以得到Fe2S3 | |
| C. | 黄铜耐腐蚀性强,不能与稀盐酸反应 | |
| D. | 某金(Au)合金的组成可表示为CuAu3.,其中金为-3价 |
11.下列离子方程式书写正确的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ | |
| D. | 金属钠跟水反应:2Na+2H2O=2Na++2OH-+H2↑ |
18.下列说法正确的是( )
| A. | 天然气、煤和石油都是清洁能源 | |
| B. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 煤的干馏是物理变化,煤的气化和液化是化学变化 | |
| D. | 液化石油气和天然气的主要成分都是甲烷 |
8.有下列物质①白磷 ②金刚石 ③co2④二氧化硅 ⑤甲烷 ⑥四氯化碳 ⑦单质硅⑧铵离子,其分子结构或晶体结构单元中存在正四面体的是( )
| A. | 除③外 | B. | 只有①⑤⑥⑧ | C. | 除③⑧外 | D. | 除③④⑦⑧ |
15.电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为 KOH 溶液,其电极反应式是:Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-..下列说法正确的是( )
| A. | Zn 为正极,Ag2O 为负极 | |
| B. | 电解质溶液中,OH-移向 Ag2O 极 | |
| C. | 锌发生还原反应,氧化银发生氧化反应 | |
| D. | 原电池工作时,正极区溶液 pH 值增大 |
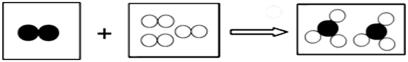
12.如下图是某化学反应的微观模型,“○”、“ ”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )
 ”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | |
| B. | 反应中共有两种元素参与 | |
| C. | 反应物和生成物中只有一种单质 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
13.下列叙述正确的是( )
| A. | 元素核外电子总倾向先排满能量较高的电子层,排满后排至能量较低的电子层? | |
| B. | 最外层电子数为1的元素一定是金属元素 | |
| C. | 原子核外M层最多容纳18个电子 | |
| D. | 镁原子与镁离子具有相同的电子层数 |
 .
.