��Ŀ����
 ���淴ӦN2+3H2 2NH3�ǹ�ҵ�Ϻϳɰ�����Ҫ��Ӧ��
���淴ӦN2+3H2 2NH3�ǹ�ҵ�Ϻϳɰ�����Ҫ��Ӧ��
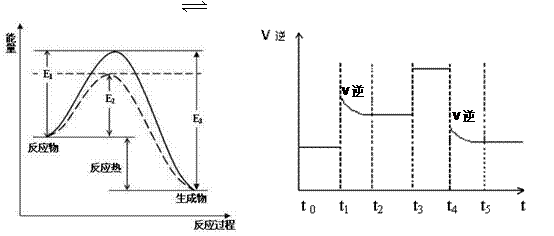
ͼ1 ��ͼ�б�ʾ����1mol����ʱ�������� ͼ2
��1������ͼ1��д���ϳɰ����Ȼ�ѧ����ʽ ��������E1��E2��E3��ʾ��
��2�� ͼ1�����߲�����ͨ���ı仯ѧ��Ӧ�е� �����������ԭ��
��
��3������Ӧ�ﵽƽ��λ��ʱ���ϸı����������ı�N2��H2��NH3��������ͼ2��ʾ��Ӧ�����뷴Ӧ���̵Ĺ�ϵ,���б�ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����
��4����һ���¶��£�����4a mol H2��2amol N2����2L���ܱ������У���ַ�Ӧ����N2��ת����Ϊ50������÷�Ӧ��ƽ�ⳣ��Ϊ ������ʱ�����������Ͷ��a mol H2��amol N2��2amol NH3���ж�ƽ���ƶ��ķ����� ���������ƶ����� �����ƶ������ƶ�����
��5��������ʵ���в�����NH3ͨ�뵽0.04mol��L-1��FeCl3��Һ�У�Ҫʹ��Һ��Fe3+���� ��
��ȫ����Fe3+Ũ�Ƚ���ԭ����ǧ��֮һ��������Һ��pHΪ ����֪�����£�Fe(OH)3��
�ܶȻ�����Ksp=4��10-38��
��14�֣���1�� N2��g��+3H2��g�� 2NH3��g�� ��H=2��E1-E3����-2(E3-E1)kg/mol ��2�֣�ûд����״̬�����֣������𰸺������֣���д��λ���۷֣�
��2�� ������2�֣��� ��Ϊ�����ܸı䷴Ӧ��·����ʹ������Ӧ����Ļ�ܽ��� ��2�֣�
��3��t 0 �C t1��2�֣� ��4��![]() ��2�֣� �����ƶ���2�֣� ��5��3 ��2�֣�
��2�֣� �����ƶ���2�֣� ��5��3 ��2�֣�

