题目内容
氯化硼(BCl3)的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A、氯化硼液态时能导电而固态时不导电 |
| B、氯化硼加到水中使溶液的pH升高 |
| C、氯化硼分子呈平面正三角形,属非极性分子 |
| D、氯化硼B-Cl之间是sp3形成的σ键 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.氯化硼是共价化合物;
B.三氯化硼水解生成HCl;
C.三氯化硼中的硼为sp2杂化,无孤对电子;
D.三氯化硼中的硼为sp2杂化.
B.三氯化硼水解生成HCl;
C.三氯化硼中的硼为sp2杂化,无孤对电子;
D.三氯化硼中的硼为sp2杂化.
解答:
解:A.氯化硼是共价化合物液态时不能导电,故A错误;
B.三氯化硼水解生成的HCl,则氯化硼加到水中使溶液的pH降低,故B错误;
C.三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,分子中正负电荷中心重叠,为非极性分子,故C正确;
D.三氯化硼中的硼原子形成3个共价键,没有孤对电子,为sp2杂化,故D错误.
故选C.
B.三氯化硼水解生成的HCl,则氯化硼加到水中使溶液的pH降低,故B错误;
C.三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,分子中正负电荷中心重叠,为非极性分子,故C正确;
D.三氯化硼中的硼原子形成3个共价键,没有孤对电子,为sp2杂化,故D错误.
故选C.
点评:本题考查原子轨道杂化,分子立体构型等,难度适中,注意三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构.

练习册系列答案
相关题目
下列说法正确的是( )
| A、冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 |
| B、“血液透析”利用了胶体的性质 |
| C、“PM2.5”是细小颗粒物悬浮在空气中形成胶体,严重危害人体健康 |
| D、电解质在水溶液和熔融状态下均能导电 |
固体酒精是目前饭桌上常用的火锅燃料,关于固体酒精燃烧过程中的叙述正确的是( )
| A、不发生状态变化 |
| B、反应中化学能转化为热能 |
| C、没有化学键断裂 |
| D、不存在氧化还原反应 |
有A、B、C三块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极;②A、C相连后,同时浸入稀H2SO4,C极发生氧化反应.则三种金属的活动性顺序为( )
| A、A>C>B |
| B、B>C>A |
| C、C>A>B |
| D、A>B>C |
 按要求对如图中两极进行必要的连接并填空:
按要求对如图中两极进行必要的连接并填空:
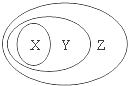 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )