题目内容
硅烷是指与烷烃结构类似,分子通式为SinH2n+2的一类化合物.其中一部分烷烃的物理性质如下表:
四种烷烃的物质性质
当n为1时称为“甲硅烷”,甲硅烷能在空气中自燃,生成无定形的二氧化硅,同时放出大量的热.
SiH4+2O2
SiO2+2H2O
请完成下列填空:
(1)短周期元素中,原子序数小于硅的主族非金属元素共有 种.短周期元素中,最外层未对电子数与硅相同的元素是(填元素符号) .与硅元素同主族的短周期元素A的氢化物与上述化学反应中两种氢化物比较,稳定性由强到弱的顺序是(用化学式表示) .
(2)上表中硅烷熔沸点递变规律是 原因是 .其中Si3H8的三氯代物分子中极性键与非极性键的个数比是 .
(3)你认为甲硅烷燃烧时除了发光发热,还可能有的实验现象是 .
(4)硅的最高价含氧酸钠盐溶于水,溶液显 性;相同条件下,该溶液与同主族、同浓度的短周期元素A的最高价含氧酸钠盐水溶液的pH(填化学式) 溶液比 溶液大.
四种烷烃的物质性质
| SiH4 | Si2H6 | Si3H8 | Si4H10 | |
| 熔点(℃) | -185 | -132.5 | -117.4 | -84.3 |
| 沸点(℃) | -111.9 | -14.5 | 52.9 | 107.4 |
| 熔点时密度(g/cm3) | 0.68 | 0.69 | 0.725 | 0.79 |
SiH4+2O2
| 点燃 |
请完成下列填空:
(1)短周期元素中,原子序数小于硅的主族非金属元素共有
(2)上表中硅烷熔沸点递变规律是
(3)你认为甲硅烷燃烧时除了发光发热,还可能有的实验现象是
(4)硅的最高价含氧酸钠盐溶于水,溶液显
考点:同一主族内元素性质递变规律与原子结构的关系,盐类水解的应用,含硅矿物及材料的应用
专题:元素周期律与元素周期表专题,盐类的水解专题
分析:(1)元素原子最外层电子数小于周期数为金属元素,据此确定每周期含有的非金属元素,结合每周期含有1种零族元素解答;
最外层未对电子数与硅相同,则元素的外围电子排布为ns2np2,或ns2np4,据此判断;
同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强氢化物越稳定;
(2)根据分子晶体的熔沸点的变化规律比较;根据Si3H8的分子中Si-Si和Si-H的数目判断;
(3)甲硅烷燃烧产物二氧化硅为固体;
(4)硅酸为弱酸,根据酸的酸性越弱,水解程度越大,对应的盐的pH越大.
最外层未对电子数与硅相同,则元素的外围电子排布为ns2np2,或ns2np4,据此判断;
同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强氢化物越稳定;
(2)根据分子晶体的熔沸点的变化规律比较;根据Si3H8的分子中Si-Si和Si-H的数目判断;
(3)甲硅烷燃烧产物二氧化硅为固体;
(4)硅酸为弱酸,根据酸的酸性越弱,水解程度越大,对应的盐的pH越大.
解答:
解:(1)元素原子最外层电子数小于周期数为金属元素,每周期含有1种零族元素,所以短周期元素中,原子序数小于硅的主族非金属元素共有6种;最外层未对电子数与硅相同,则元素的外围电子排布为ns2np2,或ns2np4,所以短周期元素中,最外层未对电子数与硅相同的元素是C、O、S;同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强氢化物越稳定,所以非金属性:O>C>Si,则其氢化物的稳定性由强到弱的顺序是H2O>CH4>SiH4,
故答案为:6;C、O、S;H2O>CH4>SiH4;
(2)硅烷是分子晶体,组成结构相似,分子晶体范德华力随式量递增而增强,所以熔沸点也相应升高;已知Si3H8的分子中含有2个Si-Si和8个Si-H,Si3H8的三氯代物分子中极性键与非极性键的个数与Si3H8相同,所以三氯代物分子中极性键与非极性键的个数比是4:1,
故答案为:随式量递增,熔沸点递增;硅烷是分子晶体,组成结构相似,分子晶体范德华力随式量递增而增强,所以熔沸点也相应升高;4:1;
(3)甲硅烷燃烧产物为二氧化硅和水,而二氧化硅为固体,所以会有白烟生成,故答案为:产生白烟;
(4)硅酸为弱酸,所以硅酸钠在溶液中水解,因而溶液显碱性;同主族非金属性越弱,则其最高价含氧酸的酸性越弱,酸性越弱,对应的钠盐的水解程度越大,对应的盐的pH越大,所以Na2SiO3溶液的pH比Na2CO3大,故答案为:碱;Na2SiO3;Na2CO3.
故答案为:6;C、O、S;H2O>CH4>SiH4;
(2)硅烷是分子晶体,组成结构相似,分子晶体范德华力随式量递增而增强,所以熔沸点也相应升高;已知Si3H8的分子中含有2个Si-Si和8个Si-H,Si3H8的三氯代物分子中极性键与非极性键的个数与Si3H8相同,所以三氯代物分子中极性键与非极性键的个数比是4:1,
故答案为:随式量递增,熔沸点递增;硅烷是分子晶体,组成结构相似,分子晶体范德华力随式量递增而增强,所以熔沸点也相应升高;4:1;
(3)甲硅烷燃烧产物为二氧化硅和水,而二氧化硅为固体,所以会有白烟生成,故答案为:产生白烟;
(4)硅酸为弱酸,所以硅酸钠在溶液中水解,因而溶液显碱性;同主族非金属性越弱,则其最高价含氧酸的酸性越弱,酸性越弱,对应的钠盐的水解程度越大,对应的盐的pH越大,所以Na2SiO3溶液的pH比Na2CO3大,故答案为:碱;Na2SiO3;Na2CO3.
点评:本题考查了元素周期表和元素周期律,涉及电子排布式,元素氢化物稳定性的比较,分子晶体熔沸点的比较,盐的水解等知识点,题目综合性较强,难度较大.

练习册系列答案
相关题目
用下列实验装置能达到实验目的是( )
A、 此图可比较 NaHCO3和 Na2CO3热稳定性大小 |
B、 此图可用铜和稀硝酸制取并收集少量 NO |
C、 此图可验证氨气易溶于水 |
D、 此图可用于实验室制取少量氨气 |
铜锌原电池(如图)工作时,下列叙述错误的是( )


| A、正极反应为:Cu2++2e-═Cu |
| B、电池反应为:Zn+Cu2+═Zn2++Cu |
| C、在外电路中,电子从负极流向正极 |
| D、盐桥中的K+移向ZnSO4溶液 |
邻甲基苯甲酸(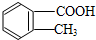 )有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
)有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
 )有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
)有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )| A、6种 | B、2种 | C、4种 | D、5种 |
“酸化”是实验中经常采用的方法,下列酸化过程正确的是( )
| A、提高高锰酸钾的氧化能力,用盐酸酸化 |
| B、抑制Fe2+的水解,用稀硝酸酸化 |
| C、检验氯代烃中含氯,加碱溶液加热后,用硫酸酸化,再检验 |
| D、确认溶液中含有SO42-时,用盐酸酸化,再检验 |
 的结构单元.B分子比A分子多了
的结构单元.B分子比A分子多了