题目内容
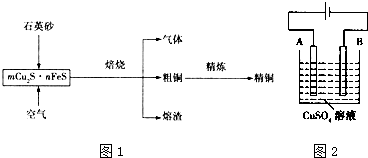
15.丙烷、乙烯等有机物在工业上有广泛的应用,回答下列问题:(1)已知下图1为各组物质能量总和及相互间转化的能量关系,写出丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3.
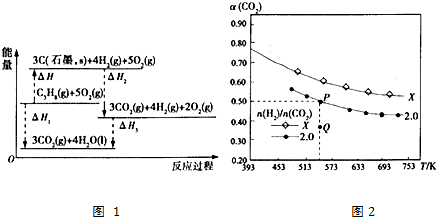
(2)在两个容积均为1L的密闭容器中以不同的氢碳比[$\frac{n({H}_{2})}{n(C{O}_{2})}$]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)△H.CO2的平衡转化率α(CO2)与温度的关系如图2所示.
①此反应的平衡常数表达式K=$\frac{{c({C_2}{H_4})•{c^4}({H_2}O)}}{{{c^2}(C{O_2})•{c^6}({H_2})}}$,P点对应温度下,K的值为64.
②该反应的△H<(填“>”“<”或“=”)0,判断的理由是温度升高CO2的平衡转化率减小,平衡逆向移动,故逆反应是吸热反应,正反应为放热反应.
③氢碳比:X>(填“>”“<”或“=”)2.0.
④在氢碳比为2.0时,Q点v(逆)<(填“>”“<”或“=”)P点的v(逆).
分析 (1)根据能量变化示意图可知,△H=△H1-(△H2+△H3);
(2)①2CO2(g)+6H2(g)?C2H4(g)+4H2O(g),所以平衡常数K=$\frac{{c({C_2}{H_4})•{c^4}({H_2}O)}}{{{c^2}(C{O_2})•{c^6}({H_2})}}$;
由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比$\frac{n({H}_{2})}{n(C{O}_{2})}$=2,设起始时氢气为2mol/L、二氧化碳为1mol/L,则二氧化碳浓度变化量为0.5mol/L,则:
2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)
起始浓度(mol/L):1 2 0 0
变化浓度(mol/L):0.5 1.5 0.25 1
平衡浓度(mol/L):0.5 0.5 0.25 1
代入平衡常数表达式计算K;
②升高温度,向吸热方向移动,根据转化率的变化来判断该反应是放热还是吸热,从而分析焓变;
③碳氢比越大,二氧化碳转化率越大;
④在氢碳比为2.0时,P点达平衡,Q点未达平衡,此时二氧化碳的转化率比平衡时小,说明此时要继续转化更多的二氧化碳,反应物浓度在减小,生成物浓度在增大,正反应速率在减小,逆反应速率在增大,所以此时逆反应速率比平衡时逆反应速率小.
解答 解:(1)根据能量变化示意图可知,丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式为:C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3,
故答案为:C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3;
(2)①2CO2(g)+6H2(g)?C2H4(g)+4H2O(g),所以平衡常数K=$\frac{{c({C_2}{H_4})•{c^4}({H_2}O)}}{{{c^2}(C{O_2})•{c^6}({H_2})}}$,
由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比$\frac{n({H}_{2})}{n(C{O}_{2})}$=2,设起始时氢气为2mol/L、二氧化碳为1mol/L,则二氧化碳浓度变化量为0.5mol/L,则:
2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)
起始浓度(mol/L):1 2 0 0
变化浓度(mol/L):0.5 1.5 0.25 1
平衡浓度(mol/L):0.5 0.5 0.25 1
代入平衡常数表达式K=$\frac{{c({C_2}{H_4})•{c^4}({H_2}O)}}{{{c^2}(C{O_2})•{c^6}({H_2})}}$=$\frac{0.25×{1}^{4}}{0.{5}^{2}×0.{5}^{6}}$=64,
故答案为:$\frac{{c({C_2}{H_4})•{c^4}({H_2}O)}}{{{c^2}(C{O_2})•{c^6}({H_2})}}$;64;
②由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应越大,则正反应为放热反应,故△H<0,
故答案为:<;温度升高CO2的平衡转化率减小,平衡逆向移动,故逆反应是吸热反应,正反应为放热反应;
③由图象可知X的碳氢比不等于2,在相同条件下反应达平衡时,二氧化碳的转化率增大了,说明是增大了氢气的量,提高二化碳的转化率,即碳氢比越大,二氧化碳转化率越大,
故答案为:>;
④在氢碳比为2.0时,P点达平衡,Q点未达平衡,此时二氧化碳的转化率比平衡时小,说明此时要继续转化更多的二氧化碳,反应物浓度在减小,生成物浓度在增大,正反应速率在减小,逆反应速率在增大,所以此时逆反应速率比平衡时逆反应速率小,
故答案为:<.
点评 本题考查热化学反应方程式的书写、化学平衡计算与影响因素、平衡常数、化学平衡图象等,侧重考查对图象的分析获取信息能力,有一定难度.

 使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).
使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液.量取10.00mL食用白醋,注入烧杯中用水稀释后转移到100mL容量瓶(填仪器名称)中定容,摇匀即得.
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂.
(3)读取盛装0.1000mol/L NaOH 溶液的碱式滴定管(填仪器名称)的初始读数.
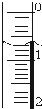
如果液面位置如右图所示,则此时的读数为0.60mL.
(4)滴定.当溶液由无色变为浅红色,并在半分钟内不褪色时,停止滴定,
并记录NaOH溶液的终读数.重复滴定3次.
Ⅱ.实验记录
| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(1)经计算,市售白醋总酸量=4.5g/100mL.
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是ab(填写序号)
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管在尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时距离摇动,有少量液体溅出.
| A. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中NH4+、Al3+、NO3-、Cl-可以共存 | |
| B. | 氧化镁可以用作耐火材料 | |
| C. | 淀粉和纤维素都可用(C6H10O5)n表示,二者互为同分异构体 | |
| D. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| A. | “歼-20”飞机上大量使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 铝合金的大量使用是因为人们能用氢气等还原剂从氧化铝中获取铝 | |
| C. | 酸碱指示剂变色、煤的液化、海水提溴、皂化反应都涉及化学变化 | |
| D. | 金属镁着火可使用干粉灭火器灭火,但不可用泡沫灭火器灭火 |
| A. | 100g 30% CH3COOH溶液中含氢原子数为2NA | |
| B. | 标准状况下,11.2 L CCl4中含有C-Cl键的数目为2NA | |
| C. | 16gO3和O2混合物中含氢原子数为NA | |
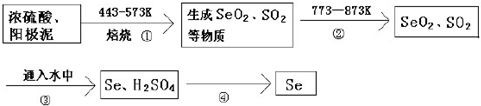
| D. | 精炼铜过程中阳极质量减少6.4g时,电路中转移电子数等于0.2NA |
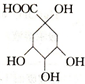
| A. | 1mol X能与5mol NaOH反应 | B. | X能发生加成、取代、氧化反应 | ||
| C. | X的分子式为C7H8O6 | D. | X与乙酸、乙醇均能发生取代反应 |
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的化学方程式为2KMnO4+5H2C2O4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O.
(2)滴定过程中操作滴定管的图示1正确的是A.
(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度偏高(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
| 试验编号 | 温度(℃) | 催化剂用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响 b.实验1和3探究反应物浓度对该反应速率的影响. c.实验2和4探究催化剂对反应速率的影响 | |
| 体积(mL) | 浓度(mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |

(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 试验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
(6)该实验中使用的催化剂应选择MnSO4并非MnCl2,原因可用离子方程式表示为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.