题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、铁与足量稀盐酸反应,1molFe失去电子数为3NA |
| B、标准状况下,22.4LH2O所含的分子数为NA |
| C、常温下,16gCH4中含有4NA个C-H键 |
| D、1mol/L的A1C13溶液中,C1-离子的数目为3 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铁与盐酸反应生成二价铁离子;
B.气体摩尔体积只适用于气体;
C.将质量转化为物质的量,结合甲烷分子的结构特点解答;
D.不知道体积,无法计算氯离子的个数.
B.气体摩尔体积只适用于气体;
C.将质量转化为物质的量,结合甲烷分子的结构特点解答;
D.不知道体积,无法计算氯离子的个数.
解答:
解:A.铁与足量稀盐酸反应生成二价铁离子,1molFe失去电子数为2NA ,故A错误;
B.标准状况下,水为液态,不能应用气体摩尔体积,故B错误;
C.16gCH4的物质的量为
=1mol,1个CH4含有4个C-H,所以16gCH4中含有4NA个C-H键,故C正确;
D.不知道体积,无法计算氯离子的个数,故D错误;
故选:C.
B.标准状况下,水为液态,不能应用气体摩尔体积,故B错误;
C.16gCH4的物质的量为
| 16g |
| 16g/mol |
D.不知道体积,无法计算氯离子的个数,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数的应用,明确以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意标准状况下物质的聚集状态.

练习册系列答案
相关题目
下列有关σ键和π键的说法错误的是( )
| A、在某些分子中,化学键可能只有π键而没有σ键 |
| B、当原子形成分子时,首先形成σ键,可能形成π键 |
| C、一般情况下,同一个分子中的σ键比π键更稳定些 |
| D、含有π键的分子在反应时,π键是化学反应的积极参与者 |
下列各仪器:①漏斗,②锥形瓶,③试管,④分液漏斗,⑤天平,⑥量筒,⑦量杯,⑧蒸馏烧瓶中常用于物质分离的仪器是( )
| A、①③⑦ | B、②⑥⑧ |
| C、①④⑧ | D、④⑥⑧ |
某气体物质,经测定其蒸气密度折合成标准状况约为1.518 g/L.该化合物可能是下列的( )
| A、HCl |
| B、H2S |
| C、CH4 |
| D、C2H6 |
在一个恒温恒容的密闭容器中发生如下反应,2A(g)+B(s)?C(g)+3D(g),不能说明该反应达到平衡的是( )
| A、气体总质量不变 |
| B、混合气体密度不变 |
| C、反应物B的浓度不变 |
| D、混合气体平均相对分子质量不再改变 |
已知有如下平衡体系:3A(g)+B(g)?2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系Ⅱ中,达平衡时体系I中A的物质的量浓度为M,体系Ⅱ中A的物质的量浓度为m,则M与m的关系为( )
| A、M=m | B、M>m |
| C、M<m | D、以上情况都有可能 |
久置的氯水中不含有的微粒是( )
| A、Cl- |
| B、HClO |
| C、H+ |
| D、H2O |
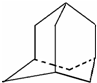 烃A分子的立体结构如图(其中C、H原子已略去);
烃A分子的立体结构如图(其中C、H原子已略去);