题目内容
7. 铁和铜是人类使用最早的金属,铁、铜及其化合物在工农业生产等许多领域中有着重要的作用.
铁和铜是人类使用最早的金属,铁、铜及其化合物在工农业生产等许多领域中有着重要的作用.(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为2Fe2++MnO2+4H+=Mn2++2Fe3++2H2O.在熔融的KOH中,O2可将Fe2(SO4)3氧化为K2 FeO4,该反应的化学方程式为2Fe2(SO4)3+20KOH+3O2=4K2FeO4+6K2SO4+10H2O.
(2)铁及其化合物可用于消除环境污染.常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时使ZnFe2Oy转变为ZnFe2O4.若2mol ZnFe2Oy与足量NO2反应可生成0.5mol N2,则y=3.
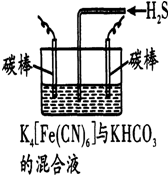
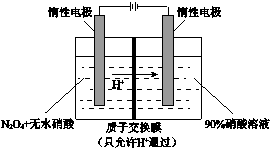
(3)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫.通电电解后通入H2S时发生反应的离子方程式为2[Fe(CN)6]3一+2CO32一+H2S=2[Fe(CN)6]4-+2HCO3-+S↓.电解时,阳极的电极反应式为[Fe(CN)6]4--e-=[Fe(CN)6]3-.
(4)在铜的冶炼过程中有如下反应发生:5FeS2+14CuSO4+12H2O═7Cu2S+5FeSO4+12H2SO4,该反应的氧化剂是FeS2和CuSO4,当有10mol FeS2参与反应时,被CuSO4氧化的为2mol.
分析 (1)二氧化锰和亚铁离子之间会发生氧化还原反应;在熔融的KOH中,O2可将Fe2(SO4)3氧化为K2 FeO4,结合质量守恒定律配平方程式;
(2)依据氧化还原反应的电子守恒计算ZnFe2Oy中Fe元素化合价,再根据化合物中的元素化合价代数为0计算y的值;
(3)电解时阳极发生失电子的氧化反应,将[Fe(CN)6]4-转化为Fe(CN)6]3-,化合价升高;
(4)反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4中,Cu元素化合价降低,被还原,CuSO4为氧化剂,FeS2中S元素化合价为-1价,反应后分别升高为+6价、降低为-2价,FeS2既是氧化剂又是还原剂,从元素化合价的角度判断并计算该题.
解答 解:(1)二氧化锰和亚铁离子之间会发生氧化还原反应,离子方程式为2Fe2++MnO2+4H+=Mn2++2Fe3++2H2O,在熔融的KOH中,O2可将Fe2(SO4)3氧化为K2 FeO4,方程式为2Fe2(SO4)3+20KOH+3O2=4K2FeO4+6K2SO4+10H2O,
故答案为:2Fe2++MnO2+4H+=Mn2++2Fe3++2H2O;2Fe2(SO4)3+20KOH+3O2=4K2FeO4+6K2SO4+10H2O;
(2)2mol ZnFe2Oy与足量NO2可生成0.5mol N2,则ZnFe2Oy被还原为ZnFe2O4,令ZnFe2Oy中铁元素的化合价为a,根据电子转移守恒,可知2mol×2×(3-a)=0.5mol×2×4,解得a=2,化合价代数和为0,则2+2×2=2y,解得y=3,
故答案为:3;
(3)电解时,阳极发生氧化反应,将[Fe(CN)6]4-转化为Fe(CN)6]3-,电极反应式为[Fe(CN)6]4--e-═[Fe(CN)6]3-,
故答案为:[Fe(CN)6]4--e-=[Fe(CN)6]3-;
(4)反应中S、Cu元素化合价降低,则FeS2和CuSO4为氧化剂,由化学方程式可知,由电子守恒可知,1mol硫酸铜得电子数为1mol,S作还原剂时化合价由-1升高到+6价,则1mol硫酸铜可以氧化$\frac{1}{7}$mol的硫,当有10mol FeS2参与反应时,有28mol硫酸铜参加反应,被CuSO4氧化的FeS2为2mol,故答案为:FeS2和CuSO4;2.
点评 本题考查氧化还原反应计算及电解等,综合性较强,注重氧化还原反应应用能力的考查,把握习题中的信息及迁移应用为解答的关键,题目难度中等.

| A. | 当一个可逆反应达到平衡状态时,这就是这个反应在该条件下所能达到的限度 | |
| B. | 可逆反应是指同一条件下,既能向正反应方向进行,又能向逆反应方向同时进行的反应 | |
| C. | 平衡状态的本质是各反应物、生成物的分子个数不再随时间改变而改变 | |
| D. | 金属钠在氧气中燃烧瞬间达到平衡状态 |
①

②
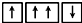
③
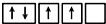
④
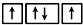
⑤
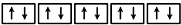
⑥

| A. | ④⑥ | B. | ②③ | C. | ②④⑤ | D. | ②③④⑥ |
| A. | 一定是m个 | B. | 一定是n个 | C. | 一定是(m+n)个 | D. | 可能是(m+n)个 |
| A. | 尽管NO2能与水反应生成硝酸,但NO2不属于酸性氧化物 | |
| B. | Na2O2粉末加入到FeSO4溶液中,产生白色沉淀,并放出大量气泡 | |
| C. | 氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应 | |
| D. | 往酸性KMnO4溶液中通入SO2验证SO2的漂白性 |
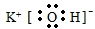 ;CO2
;CO2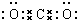 .
.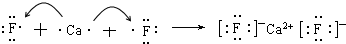 .
.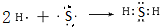 .
. 氮氧化物(NOx)种类很多,造成大气污染的主要是NO和NO2,研究它们的综合利用有重要意义.
氮氧化物(NOx)种类很多,造成大气污染的主要是NO和NO2,研究它们的综合利用有重要意义. 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题: (填电子式),B
(填电子式),B (填结构式),E
(填结构式),E (填结构简式).
(填结构简式).