题目内容
16.下列有关醇的叙述正确的是( )| A. | 所有醇都能发生催化氧化、消去反应 | |
| B. | 低级醇(甲醇、乙醇、丙醇、乙二醇)都能与水以任意比互溶 | |
| C. | 凡烃基直接和羟基相连的化合物一定是醇 | |
| D. | 乙醇和浓硫酸按1:3体积比混合、共热就一定产生乙烯. |
分析 A.甲醇不能发生消去反应,与-OH相连的C上没有H不能发生催化氧化,与-OH相连C的邻位C上没有H不能发生消去反应;
B.低级醇含-OH与水形成氢键;
C.苯酚与羟基相连为酚类物质;
D.乙醇与浓硫酸加热至170℃发生消去反应.
解答 解:A.甲醇不能发生消去反应,与-OH相连的C上没有H不能发生催化氧化,与-OH相连C的邻位C上没有H不能发生消去反应,则醇不一定能发生催化氧化和消去反应,应符合结构特点,故A错误;
B.低级醇含-OH与水形成氢键,则都能与水以任意比互溶,故B正确;
C.苯酚与羟基相连为酚类物质,羟基与脂肪烃基相连的为醇,故C错误;
D.乙醇与浓硫酸加热至170℃发生消去反应生成乙烯,在140℃发生取代反应生成乙醚,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意醇的消去、氧化反应的结构特点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列关于明矾[KAl(SO4)2•12H2O]溶液的叙述正确昀是( )
| A. | 明矾净水原理为:Al3++3H2O=Al(OH)3↓+3H+ | |
| B. | 该溶液中AlO2-、F-、K+、Na+能大量共存 | |
| C. | 加入过量NH3•H2O反应的离子方程式为:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| D. | 加入过量Ba(OH)2溶液反应的离子方程式为:Al3++2SO42-+4OH-+2Ba2+=AlO2-十2BaSO4↓+2H2O |
4.饱和醇(X)与足量乙酸反应生成酯(Y),相对分子质量满足Mr(Y)=Mr(X)+42,X的相对分子质量为90,且X可由烯烃与水在一定条件下反应制得.Y的结构共有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
11.将镁、铜组成的合金1.28g投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物只有NO气体0.672L(标准状况),向反应后的溶液中加入足量的NaOH溶液.则形成沉淀的质量为2.81g.
8. 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
则A原子的价电子排布式为3s2.
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
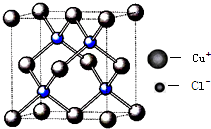
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
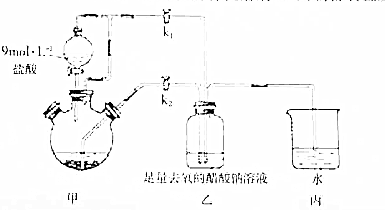 ①检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液.
①检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液.