题目内容
聚甲基丙烯酸羟乙酯的结构简式为 ,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
(1)由甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯
(2)由甲基丙烯酸制备甲基丙烯酸羟乙酯
(3)由乙烯制备乙二醇 .
 ,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:(1)由甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯
(2)由甲基丙烯酸制备甲基丙烯酸羟乙酯
(3)由乙烯制备乙二醇
考点:有机物的合成,有机物的结构和性质
专题:有机物的化学性质及推断
分析:(1)甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯,发生加聚反应生成高分子化合物;
(2)由甲基丙烯酸制备甲基丙烯酸羟乙酯,发生酯化反应;
(3)由乙烯制备乙二醇,先发生与溴水的加成,然后在水解生成乙二醇.
(2)由甲基丙烯酸制备甲基丙烯酸羟乙酯,发生酯化反应;
(3)由乙烯制备乙二醇,先发生与溴水的加成,然后在水解生成乙二醇.
解答:
解:(1)甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯,发生加聚反应生成高分子化合物,该加聚反应为nCH2=C(CH3)COOCH2CH2OH
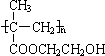 ,
,
故答案为:nCH2=C(CH3)COOCH2CH2OH
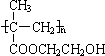 ;
;
(2)由甲基丙烯酸制备基丙烯酸羟乙酯,可与乙二醇发生酯化反应,该反应为CH2=C(CH3)COOH+HOCH2CH2OH
CH2=C(CH3)COOCH2CH2OH+H2O,
故答案为:CH2=C(CH3)COOH+HOCH2CH2OH
CH2=C(CH3)COOCH2CH2OH+H2O;
(3)由乙烯制备乙二醇,先发生与溴水的加成,然后再水解生成乙二醇,发生的反应分别为CH2=CH2+Br2→CH2Br-CH2Br、CH2Br-CH2Br+2NaOH
HOCH2CH2OH+2NaBr,
故答案为:CH2=CH2+Br2→CH2Br-CH2Br、CH2Br-CH2Br+2NaOH
HOCH2CH2OH+2NaBr.
| 催化剂 |
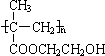 ,
,故答案为:nCH2=C(CH3)COOCH2CH2OH
| 催化剂 |
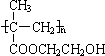 ;
;(2)由甲基丙烯酸制备基丙烯酸羟乙酯,可与乙二醇发生酯化反应,该反应为CH2=C(CH3)COOH+HOCH2CH2OH
| 催化剂 |
| △ |
故答案为:CH2=C(CH3)COOH+HOCH2CH2OH
| 催化剂 |
| △ |
(3)由乙烯制备乙二醇,先发生与溴水的加成,然后再水解生成乙二醇,发生的反应分别为CH2=CH2+Br2→CH2Br-CH2Br、CH2Br-CH2Br+2NaOH
| 水 |
| △ |
故答案为:CH2=CH2+Br2→CH2Br-CH2Br、CH2Br-CH2Br+2NaOH
| 水 |
| △ |
点评:本题考查有机物的制备及结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、羧酸、卤代烃性质的考查,注意有机合成中发生的反应,题目难度不大.

练习册系列答案
相关题目
下列各组离子,能在强酸溶液中大量共存.并且溶液呈无色的是( )
| A、Mg2+、Na+、SO42-、Cl- |
| B、K+、Na+、NO3-、MnO4- |
| C、Na+、Ca2+、OH-、HCO3- |
| D、NH4+、Cu2+、NO3-、Cl- |

 现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题:
现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题: 如图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质.已知:①I是一种常见的温室气体,E原子核内有12个质子②G是一种红棕色固体粉末,反应C+G
如图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质.已知:①I是一种常见的温室气体,E原子核内有12个质子②G是一种红棕色固体粉末,反应C+G
