题目内容
7.下列各组分子中,中心原子杂化轨道的类型不相同的是( )| A. | CO2与SO2 | B. | CH4与NH3 | C. | SO3与BF3 | D. | H2S与CCl4 |
分析 根据价层电子对互斥理论确定中心原子杂化类型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.根据n值判断杂化类型:一般有如下规律:当n=2,sp杂化;n=3,sp2杂化;n=4,sp3杂化.
解答 解:A.CO2中C形成2个σ键,无孤电子对,为sp杂化,SO2中S形成2个δ键,孤电子对数=$\frac{6-2×2}{2}$=1,为sp2杂化,中心原子杂化轨道的类型不相同,故A正确;
B.CH4中C形成4个σ键,无孤电子对,为sp3杂化,NH3中N形成3个σ键,孤电子对数=$\frac{5-3×1}{2}$=1,为sp3杂化,中心原子杂化轨道的类型相同,故B错误;
C.SO3中S原子杂化轨道数为$\frac{1}{2}$(6+0)=3,采取 sp2杂化方式,BF3中B原子杂化轨道数为$\frac{1}{2}$(3+3)=3,采取 sp2杂化方式,中心原子杂化轨道的类型相同,故C错误;
D.H2S分子中S原子价层电子对个数=2+$\frac{1}{2}$×(6-2×1)=4,所以采用sp3杂化;CCl4分子中价层电子对个数=2+$\frac{1}{2}$(4-4×1)=4,所以采用sp3杂化,中心原子杂化轨道的类型相同,故D错误;
故选A.
点评 本题考查原子杂化方式判断,为高频考点,明确价层电子对互斥理论即可解答,难点是孤电子对计算方法,题目难度中等.

练习册系列答案
相关题目
15.在溶液中能大量共存的离子组是( )
| A. | Fe3+、OH一、HCO3- | B. | Ba2+、OH一、C1- | C. | H+、K+、CO32-、 | D. | NH4+、NO3-、OH- |
15.下列叙述中正确的是( )
| A. | 液态HBr不导电,因此HBr是非电解质 | |
| B. | 强电解质溶液的导电性不一定很强 | |
| C. | NH3的水溶液能导电,因此NH3是电解质 | |
| D. | 强电解质在液态时一定能导电 |
12.下列关于苯酚的叙述不正确的是( )
| A. | 苯酚是一种弱酸,滴加指示剂会变色 | |
| B. | 苯酚在水溶液中能按下式电离: | |
| C. | 苯酚钠水溶液里通入CO2气体总是生成NaHCO3 | |
| D. | 苯酚有腐蚀性,溅在皮肤上可用酒精冲洗 |
16.下列物质中,与NaOH溶液、Na2CO3、溴水、苯酚钠水溶液和甲醇都能反应的是( )
| A. | 苯 | B. | CH3CHO | C. | CH3COOH | D. | CH2=CH-COOH |
17.有6种物质按下列顺序排列:①X ②Cl2 ③HClO ④KClO3 ⑤KClO4 根据它们这种排列规律,X应该是下列中的( )
| A. | HClO3 | B. | CaCl2 | C. | Cl2O7 | D. | Cl2O3 |
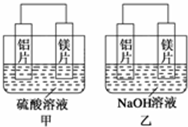 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示.
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示.