题目内容
同温同压下,同体积的N2和SO2分子数之比为 ,物质的量之比为 ,原子总数之比为 ,摩尔质量之比为 ,质量之比为 ,密度之比为 。
1∶1 ,1∶1 ,2∶3 ,7∶16 , 7∶16 ,7∶16 。
【解析】
试题分析:同温同压下,同体积的N2和SO2的物质的量相等,所以分子数也相等,二者的分子数之比为1:1;物质的量之比是1:1;由于N2是双原子分子,而SO2是三原子分子,所以当二者分子数相等时,原子总数之比为就是分子内原子个数之比,是2:3;摩尔质量之比就是二者的相对分子质量之比,为7∶16 ,由于它们的物质的量相等,根据m=n·M可知二者的质量之比7∶16;由于气体的密度ρ=m÷V=M÷Vm,在相同的外界条件下,气体摩尔体积相等,所以气体的密度之比为二者的相对分子质量之比,是7∶16 。
考点:考查阿伏伽德罗定律及推论的应用的知识。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下述实验不能达到预期实验目的的是( )
序号 | 实验内容 | 实验目的 |
A | 将2.5gCuSO4·5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
 2CO(g)⊿H=+QkJ/mol,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的 ( )
2CO(g)⊿H=+QkJ/mol,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的 ( )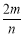 B.
B.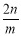 C.
C.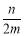 D.
D.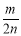
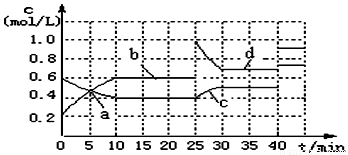
 N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )