题目内容
下列各组离子在给定条件下能大量共存的是( )
A、在pH=1的溶液中:NH
| ||||
B、有NO3-存在的强酸性溶液中:NH
| ||||
C、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、AlO
| ||||
D、有SO
|
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液呈酸性,与氢离子反应的离子不能大量共存;
B.有NO3-存在的强酸性溶液具有强氧化性,具有还原性的离子不能大量共存;
C.c(H+)=1.0×10-13mol?L-1的溶液呈碱性;
D.与SO42-反应的离子不能大量共存.
B.有NO3-存在的强酸性溶液具有强氧化性,具有还原性的离子不能大量共存;
C.c(H+)=1.0×10-13mol?L-1的溶液呈碱性;
D.与SO42-反应的离子不能大量共存.
解答:
解:A.pH=1的溶液呈酸性,ClO-与氢离子反应生成弱酸而不能大量共存,故A错误;
B.有NO3-存在的强酸性溶液具有强氧化性,具有还原性的Fe2+、Br-不能大量共存,故B错误;
C.c(H+)=1.0×10-13mol?L-1的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.Ba2+与SO42-反应生成沉淀而不能大量共存,故D错误.
故选C.
B.有NO3-存在的强酸性溶液具有强氧化性,具有还原性的Fe2+、Br-不能大量共存,故B错误;
C.c(H+)=1.0×10-13mol?L-1的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.Ba2+与SO42-反应生成沉淀而不能大量共存,故D错误.
故选C.
点评:本题考查离子共存问题,为高考常见题型,侧重于学生的元素化合价知识的考查与应用,难度不大,注意把握题目所给信息,答题时注意审题,注意把握常见离子的性质以及反应类型的判断.

练习册系列答案
相关题目
某同学想对MnO2、CuO、Fe2O3、Cr2O3在氯酸钾分解反应中的催化作用进行如下实验:
下列叙述不正确的是( )
| 实验 编号 |
KClO3(g) | 氧化物 | 产生气体(mL) (已折算为标况) |
耗时(s) | ||
| 化学式 | 质量(g) | 实际回收 | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2(有刺激性气味) | 188.3 |
| A、催化剂的催化能力Fe2O3>MnO2>CuO |
| B、实验2、3、4中KClO3分解百分率相同 |
| C、实验1设计对本实验无意义 |
| D、Cr2O3在反应中起到还原剂作用 |
如图所示与对应的叙述相符的是( )
A、 四种基本反应类型与氧化还原反应的关系 |
B、 AlCl3溶液滴加NaOH溶液生成沉淀的情况 |
C、 Ba(OH)2溶液中滴加硫酸溶液导电性的情况 |
D、 等体积等浓度稀硫酸分别与足量铁和镁反应的情况 |
下列叙述正确的是( )
| A、金属与盐溶液反应都是置换反应 |
| B、阴离子都只有还原性 |
| C、与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
| D、在潮湿的环境下,黄铜(锌铜合金)比纯铜更耐腐蚀 |
对于下列反应的反应类型的判断,不正确的是( )
A、CO2+H2O
| ||||
B、Cu(OH)2
| ||||
C、Fe2O3+3CO
| ||||
| D、NaCl+AgNO3═AgCl↓+NaNO3复分解反应 |
能正确表示四种基本类型反应与氧化反应关系的示意图是( )
A、 |
B、 |
C、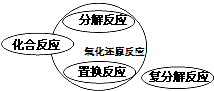 |
D、 |
 分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )
分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )| A、化合反应 | B、氧化还原反应 |
| C、可逆反应 | D、置换反应 |
等质量的下列物质完全燃烧时,消耗氧气的量最多的是( )
| A、C2H4 |
| B、C6H6 |
| C、C2H5OH |
| D、CH3COOH |
实验室中需要配制1mol/L的NaCl溶液448mL,配置时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、448mL 26.2g |
| B、500mL 29.3g |
| C、1000mL 29.3g |
| D、450mL 26.2g |