题目内容
15.下列说法正确的是( )| A. | 将二氧化硫通入到紫色石蕊溶液中,溶液先变红后褪色 | |
| B. | 原电池工作时负极质量一定减少 | |
| C. | 红热的铁与水蒸气反应生成氧化铁和氢气 | |
| D. | 石油的分馏属于物理变化,煤的干馏属于化学变化 |
分析 A.二氧化硫通入到紫色石蕊溶液中,石蕊遇酸变红;
B.燃料电池的负极材料不变;
C.Fe与水蒸气反应生成四氧化三铁和氢气;
D.分馏与混合物的沸点有关,干馏为煤在隔绝空气条件下发生的复杂物理化学变化,生成煤焦油等.
解答 解:A.二氧化硫通入到紫色石蕊溶液中,石蕊遇酸变红,体现其酸性氧化物的性质,与漂白性无关,故A错误;
B.燃料电池的负极材料不变,则原电池的负极不一定减少,故B错误;
C.Fe与水蒸气反应生成四氧化三铁和氢气,四氧化三铁为黑色,故C错误;
D.分馏与混合物的沸点有关,干馏为煤在隔绝空气条件下发生的复杂物理化学变化,生成煤焦油等,前者为物理变化,后者为化学变化,故D正确;
故选D.
点评 本题考查物质的性质及反应原理,为高频考点,把握物质的性质、发生的反应、原电池等为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.实验室配制250mL物质的量浓度为1.0mol•L-l H2SO4溶液 时,下列仪器不需要的是( )
| A. | 托盘天平 | B. | 胶头滴管 | C. | 250 mL容量瓶 | D. | 量筒 |
20.根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是( )
I2+SO2+2H2O═H2SO4+2HI
2FeCl2+Cl2═2FeCl3
2FeCl3+2HI═2FeCl2+2HCl+I2.
I2+SO2+2H2O═H2SO4+2HI
2FeCl2+Cl2═2FeCl3
2FeCl3+2HI═2FeCl2+2HCl+I2.
| A. | SO2>I->Fe2+ | B. | I->Fe2+>SO2 | C. | Fe2+>I->SO2 | D. | Fe2+>SO2>I- |
4.1mol SO2和1mol SO3具有相同的:①分子数 ②原子总数 ③硫原子数 ④氧原子数( )
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ①②③ |
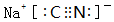 .
.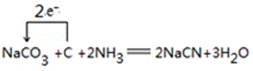 .
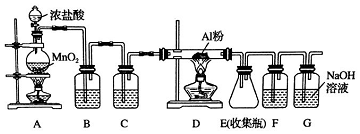
.
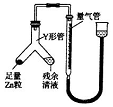
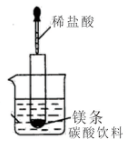 (1)如图所示(夹持仪器省去),把试管放入盛有20℃碳酸饮料的烧杯中,试管中开始放入几块镁条,再用滴管滴加5ml的盐酸于试管中.
(1)如图所示(夹持仪器省去),把试管放入盛有20℃碳酸饮料的烧杯中,试管中开始放入几块镁条,再用滴管滴加5ml的盐酸于试管中.