题目内容
氯气及其化合物在工农业生产和人类生活中都有着重要的应用.
(1)Ca(ClO)2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有 性,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式 .
(2)棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,配平并补充完整下列反应方程式:
Cl2+ Na2CO3+ = NaHCO3+ NaCl+ Cl2O
(3)黄色气体ClO2可用于污水杀菌和饮用水净化.
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为 .
②ClO2遇浓盐酸会生成Cl2,每生成1mol Cl2转移电子的物质的量为 .
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为 .
(4)用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应4HCl+O2
2Cl2+2H2O,可实现氯的循环利用.
已知:①上述反应中,4mol HCl被氧化放出115.6kJ的热量.
②
则断开1mol H-O键与断开1mol H-Cl键所需能量相差约为 kJ,H2O中H-O键比HC1中H-Cl键(填“强”或“弱”) .
(1)Ca(ClO)2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有
(2)棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,配平并补充完整下列反应方程式:
(3)黄色气体ClO2可用于污水杀菌和饮用水净化.
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为
②ClO2遇浓盐酸会生成Cl2,每生成1mol Cl2转移电子的物质的量为
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(4)用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应4HCl+O2
| CuO、CuCl2 |
| 400℃ |
已知:①上述反应中,4mol HCl被氧化放出115.6kJ的热量.
②

则断开1mol H-O键与断开1mol H-Cl键所需能量相差约为
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:(1)次氯酸盐具有强氧化性,可起到杀菌消毒的作用;氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水;
(2)结合质量守恒和电子守恒配平方程式;
(3)①KClO3与SO2在强酸性溶液中反应可制得ClO2,同时应生成硫酸钾;
②ClO2遇浓盐酸会生成Cl2,同时生成水,写出反应的方程式,根据方程式计算;
③可从电子得失守恒的角度计算,也可写出方程式计算;
(4)根据反应热等于反应物总键能减生成物总键能计算.
(2)结合质量守恒和电子守恒配平方程式;
(3)①KClO3与SO2在强酸性溶液中反应可制得ClO2,同时应生成硫酸钾;
②ClO2遇浓盐酸会生成Cl2,同时生成水,写出反应的方程式,根据方程式计算;
③可从电子得失守恒的角度计算,也可写出方程式计算;
(4)根据反应热等于反应物总键能减生成物总键能计算.
解答:
解:(1)次氯酸盐具有强氧化性,可起到杀菌消毒的作用;氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=ClO-+Cl-+H2O,
故答案为:强氧化;Cl2+2OH-=ClO-+Cl-+H2O;
(2)依据氧化还原反应的元素化合价变化,结合电子守恒和原子守恒确定空项物质,反应中氯气是自身氧化还原反应,化合价从0价变化为-1价和+1价;依据原子守恒进而电子守恒得到,反应物缺项为H2O;配平的化学方程式为:2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O,
故答案为:2;2;H2O;2;2;1;
(3)①KClO3与SO2在强酸性溶液中反应可制得ClO2,同时应生成硫酸钾,反应的离子方程式为2ClO3-+SO2=2ClO2+SO42-,故答案为:2ClO3-+SO2=2ClO2+SO42-;
②ClO2遇浓盐酸会生成Cl2,同时生成水,反应的化学方程式为2ClO2+8HCl=5Cl2+4H2O,由方程式可知,当生成5molCl2,转移8mol电子,则生成1mol Cl2转移电子的物质的量为1.6mol,
故答案为:1.6mol;
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,反应中ClO2为氧化剂,Cl元素化合价由+4价降低为-1价,Mn2+为还原剂,元素化合价由+2价升高到+4价,氧化剂和还原剂得失电子数目相等,则氧化剂和还原剂的物质的量之比为2:5,
故答案为:2:5;
(4)E(H-O)、E(HCl)分别表示H-O键能、H-Cl键能,
反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:
4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+2×E(H-O)]=-115.6KJ/mol,
整理得,4E(H-Cl)-4E(H-O)=-127.6kJ/mol,即E(H-O)-E(HCl)=31.9kJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ/mol×1mol=31.9kJ,
键能越大,则越稳定,
故答案为:31.9;强.
故答案为:强氧化;Cl2+2OH-=ClO-+Cl-+H2O;
(2)依据氧化还原反应的元素化合价变化,结合电子守恒和原子守恒确定空项物质,反应中氯气是自身氧化还原反应,化合价从0价变化为-1价和+1价;依据原子守恒进而电子守恒得到,反应物缺项为H2O;配平的化学方程式为:2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O,
故答案为:2;2;H2O;2;2;1;
(3)①KClO3与SO2在强酸性溶液中反应可制得ClO2,同时应生成硫酸钾,反应的离子方程式为2ClO3-+SO2=2ClO2+SO42-,故答案为:2ClO3-+SO2=2ClO2+SO42-;
②ClO2遇浓盐酸会生成Cl2,同时生成水,反应的化学方程式为2ClO2+8HCl=5Cl2+4H2O,由方程式可知,当生成5molCl2,转移8mol电子,则生成1mol Cl2转移电子的物质的量为1.6mol,
故答案为:1.6mol;
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,反应中ClO2为氧化剂,Cl元素化合价由+4价降低为-1价,Mn2+为还原剂,元素化合价由+2价升高到+4价,氧化剂和还原剂得失电子数目相等,则氧化剂和还原剂的物质的量之比为2:5,
故答案为:2:5;
(4)E(H-O)、E(HCl)分别表示H-O键能、H-Cl键能,
反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:
4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+2×E(H-O)]=-115.6KJ/mol,
整理得,4E(H-Cl)-4E(H-O)=-127.6kJ/mol,即E(H-O)-E(HCl)=31.9kJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ/mol×1mol=31.9kJ,
键能越大,则越稳定,
故答案为:31.9;强.
点评:本题以氯气的性质为载体综合考查学生的分析能力和实验能力,为高考常见题型和高频考点,注意把握物质的性质以及实验原理的理解,难度中等.

练习册系列答案
相关题目
 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是( )| A、有反应CO32-+2H+=CO2↑+H2O发生 |
| B、有反应CO32-+H+=HCO3-发生 |
| C、有反应CO32-+CO2+H2O=2HCO3-发生 |
| D、加快盐酸注入速度不会改变反应现象 |
下列离子方程式中,书写正确的是( )
| A、铝与盐酸反应:Al+H+=Al3++H2↑ |
| B、氢氧化铝与氢氧化钠溶液反应:Al(OH)3+OH-=AlO2-+2H2O |
| C、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
| D、铝与氢氧化钠溶液反应:Al+2 OH-=AlO2-+H2↑ |
NA代表阿伏加德罗常数,以下说法正确的是( )
| A、在25°C、1.01×105Pa时,11.2氮气所含的原子数目为NA |
| B、18g水所含的电子数目为NA |
| C、121gCCl2F2所含的氯原子数为2NA |
| D、醋酸的摩尔质量与NA个醋酸分子的质量在数值上不相等 |
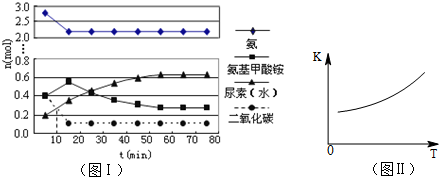
 工业上利用CO和水蒸气在一定条件下发生反应制取氢气.
工业上利用CO和水蒸气在一定条件下发生反应制取氢气.