题目内容
20.用酸式滴定管准确移取20.00mL某未知浓度的硫酸于一洁净的锥形瓶中,然后用0.20mol/L的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
(2)以下操作可能造成测定结果偏低的是B(填写序号).
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.滴定管在滴定前尖嘴处有气泡,滴定后消失
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管.
分析 (1)根据硫酸和氢氧化钠恰好反应,二者的关系H2SO4~2NaOH求出硫酸的浓度,氢氧化钠的体积取平均值,考虑到第三次误差较大,应舍去;
(2)根据操作对c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$的影响进行分析误差.
解答 解:(1)氢氧化钠的体积第三次误差较大,应舍去,其余3次的平均体积为:(18.30+18.10+18.20)mL÷3=18.20mL,硫酸和氢氧化钠恰好反应的关系:
H2SO4~2NaOH,则硫酸的物质的量为:$\frac{1}{2}$×18.20×10-3L×0.20mol/L=1.82×10-3mol,浓度c=$\frac{n}{V}$=$\frac{1.82×1{0}^{-3}mol}{20.00×1{0}^{-3}L}$=0.091mol/L,
故答案为:0.091;
(2)根据c(H2SO4)=$\frac{c(NaOH)×V(NaOH)}{2V({H}_{2}S{O}_{4})}$分析:
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质,导致所用氢氧化钠溶液体积偏大,造成测定结果偏高,故A偏高;
B.滴定终点读数时,俯视滴定管的刻度,其读数偏少,V(NaOH)偏少,故B偏低;
C.滴定管在滴定前尖嘴处有气泡,滴定后消失,V(NaOH)偏高,故C偏高;
D.实验目的是中和已定量的硫酸,与锥形瓶中水的多少无关,所以盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,对实验无影响,故D无影响;
E.未用标准液润洗碱式滴定管,氢氧化钠浓度降低,导致所用氢氧化钠体积增多,故E偏高;
故答案为:B.
点评 本题考查中和滴定量实验,明确实验原理和判断错误操作导致消耗标准液体积的影响是解题关键,注意在计算所用标准溶液的体积时,把不合理的数据去掉,剩余数据取平均值,题目难度中等.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案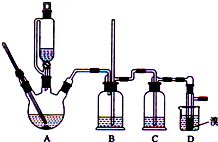 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
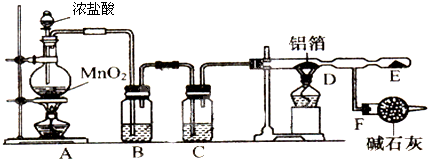
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是D;(填正确选项前的字母)
A.引发反应 B.加快反应速度 C.防止乙醇挥发 D.减少副产物乙醚生成
(2)在装置C中应加入C,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
A.水 B.浓硫酸 C.氢氧化钠溶液 D.饱和碳酸氢钠溶液
(3)判断该制备实验中各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗(填仪器名)中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用B洗涤除去;(填正确选项前的字母)
A.水 B.氢氧化钠溶液 C.碘化钠溶液 D.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是冷却,避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
| A. | 恒温恒容,充入NO2气体,其转化率增大 | |
| B. | 加压,平衡向逆反应方向移动,混合气体颜色变深 | |
| C. | 若平衡常数增大,则可能是升高了温度或减小了体系的压强 | |
| D. | 当2v正(NO)=v逆(O2)时,反应达到化学平衡状态 |
| A. | 0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol | |
| B. | 将Na2O2粉末加入到饱和NaOH溶液中,OH-离子浓度一定不变 | |
| C. | 等物质的量的Na2O2与Na2O溶于等质量水中得到的NaOH的物质的量浓度相同 | |
| D. | 等质量的Na2O2与Na2S晶体中含有相同数目的阴离子 |
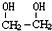 )是一种重要的化工原料,
)是一种重要的化工原料, (g)△H=a kJ/mol
(g)△H=a kJ/mol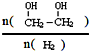 增大的措施有降温、加压、增加CO的浓度或及时将乙二醇从混合物中分离出来(写两条)
增大的措施有降温、加压、增加CO的浓度或及时将乙二醇从混合物中分离出来(写两条)