题目内容
A、B、C、D四种元素,A元素所处的周期数,主族序数,原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称
(2)A、B形成的化合物的电子式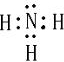
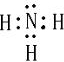 ;
;
(3)C的元素符号
(4)D的最高价氧化物的水化物中含有
(5)用电子式表示D2C的形成过程:
 .
.
(1)B元素的名称
氮
氮
,B在周期表中的位置第二周期第VA族
第二周期第VA族
,(2)A、B形成的化合物的电子式
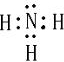
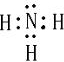
(3)C的元素符号
S
S
,C的最高价氧化物的化学式SO3
SO3
;(4)D的最高价氧化物的水化物中含有
离子键、共价键
离子键、共价键
键.(5)用电子式表示D2C的形成过程:


分析:A元素所处的周期数,主族序数,原子序数均相等,则A为H;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B为N;C元素原子的最外层电子数比次外层少2个,C有3个电子层,最外层电子数为6,则C为S;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C,则D在第四周期第ⅠA族,即D为K,然后利用元素及其单质、化合物的性质来解答.
解答:解:A元素所处的周期数,主族序数,原子序数均相等,则A为H;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B为N;C元素原子的最外层电子数比次外层少2个,C有3个电子层,最外层电子数为6,则C为S;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C,则D在第四周期第ⅠA族,即D为K,
(1)B为N,其名称为氮,原子结构中有2个电子层,最外层电子数为5,故答案为:氮;第二周期第VA族;
(2)A、B形成的化合物为NH3,其电子式为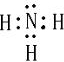 ,故答案为:
,故答案为: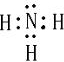 ;
;
(3)C的元素符号为S,最高价为+6价,则最高价氧化物为SO3,故答案为:S;SO3;
(4)D的最高价氧化物的水化物为KOH,含有离子键、共价键,故答案为:离子键、共价键;
(5)K最外层1个电子,S最外层6个电子,则用电子式表示K2S的形成过程为 ,
,
故答案为: .
.
(1)B为N,其名称为氮,原子结构中有2个电子层,最外层电子数为5,故答案为:氮;第二周期第VA族;
(2)A、B形成的化合物为NH3,其电子式为
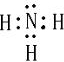 ,故答案为:
,故答案为: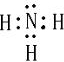 ;
;(3)C的元素符号为S,最高价为+6价,则最高价氧化物为SO3,故答案为:S;SO3;
(4)D的最高价氧化物的水化物为KOH,含有离子键、共价键,故答案为:离子键、共价键;
(5)K最外层1个电子,S最外层6个电子,则用电子式表示K2S的形成过程为
 ,
,故答案为:
 .
.点评:本题考查位置、结构、性质的应用,元素的推断是解答的关键,明确元素的性质、元素在周期表中的位置、利用化学式分析化合价等即可解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目




 ,B、C可形成离子化合物
,B、C可形成离子化合物 ,B、C可形成离子化合物
,B、C可形成离子化合物