题目内容
11.理论上,不能设计为原电池的化学反应是( )| A. | 2H2(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2H2O(l)△H<0 | B. | 2FeCl3(aq)+Fe(s)═3FeCl2(aq)△H<0 | ||
| C. | CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)+2H2O(l)△H<0 | D. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H<0 |
分析 自发的氧化还原反应能设计成原电池,复分解反应不能设计成原电池,根据反应的类型判断.
解答 解:A、2H2(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2H2O(l)△H<0,该反应属于自发的氧化还原反应,所以能设计成原电池,故A不选;
B、2FeCl3+Fe═3FeCl2,该反应属于自发的氧化还原反应,所以能设计成原电池,故B不选;
C、CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)+2H2O(l)△H<0,该反应属于自发的氧化还原反应,所以能设计成原电池,故C不选;
D、HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H<0,该反应属于复分解反应,不是氧化还原反应,所以不能设计成原电池,故D选;
故选D.
点评 本题考查学生设计成原电池的反应应具备的条件,难度不大,根据原电池的构成条件进行设计原电池即可.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
19.反应3ClO-+2Fe3++10OH-═2FeO42-+5H2O+3Cl-,下列有关该反应的说法中正确的是( )
| A. | ClO-作氧化剂 | |
| B. | FeO42-为还原产物 | |
| C. | 每产生1 mol FeO42-,转移3 mol电子 | |
| D. | OH-作氧化剂 |
16.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA | |
| B. | 7 g CnH2n中含有的氢原子数目为NA | |
| C. | 任何气体单质在标况下体积若为22.4L,则含有2NA个原子 | |
| D. | 1mol Na2O2与水反应转移的电子数约为1.204×1024个 |
3.将质量分数为14%的Ba(OH)2溶液加热蒸发掉50g水后,得到质量分数为21%的溶液80mL,此时溶液的物质的量浓度约为( )
| A. | 1.08mol•L-1 | B. | 1.37mol•L-1 | C. | 1.54mol•L-1 | D. | 2.48mol•L-1 |
11.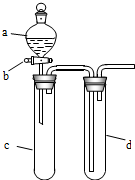 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是检查装置气密性.
(2)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是丙.
(3)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,再由a向c中加2mL蒸馏水,c中的实验现象是反应变缓,气体颜色变淡.
 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是检查装置气密性.
(2)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是丙.
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
12.将K、SiO2、Na2O、NaOH、NaHSO4分别加热熔化,需要克服相同类型作用力的物质有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |