题目内容
11.请根据下列信息判断氢气燃烧生成水蒸气时的量变化.下列有关叙述正确的是( )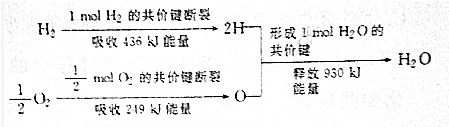
| A. | 氢气燃烧生成水蒸气时吸收热量 | |
| B. | 生成1molH2O吸收热量245kJ | |
| C. | 2molH和1molO所具有的能量大于1molH2和$\frac{1}{2}$molO2所具有的总能量 | |
| D. | 氢气和氧气的总能量大于水的能量 |
分析 上图表示了1mol氢气和0.5mol氧气反应生成1mol水的过程中的能量变化,断键吸收能量,成键释放能量,△H=反应物键能和-生成物键能和,据此解答.
解答 解:△H=反应物键能和-生成物键能和=436KJ/mol+249KJ/mol-930KJ/mol=-245KJ/mol,
A.氢气燃烧生成水是放热反应,反应过程中放出热量,故A错误;
B.生成1molH2O放出热量=930KJ-436KJ-249KJ=245kJ,故B错误;
C.氢气吸收能量变化为氢原子,氧气吸收能量变化为氧原子,所以2molH和1molO所具有的能量大于1molH2和$\frac{1}{2}$molO2所具有的总能量,故C正确;
D.氢气燃烧是放热反应,反应物能量高于生成物的能量,1mol氢气和$\frac{1}{2}$mol氧气的总能量大于1mol水的能量,选项中未指明物质的量,不能确定能量大小,故D错误;
故选C.
点评 本题考查了氢气和氧气生成水的过程中的能量变化,注意△H=反应物键能和-生成物键能和,题目难度不大.

练习册系列答案
相关题目
1.下列关于反应热的说法正确的是( )
| A. | 当△H<0时,表示该反应为吸热反应 | |
| B. | 反应热与物质在反应时的状态有关 | |
| C. | 已知C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol | |
| D. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
2.下列有关概念的说法正确的是( )
| A. | 阿伏伽德罗常数就是6.02×1023 mol-1 | |
| B. | 摩尔质量就是1 mol物质的质量 | |
| C. | 物质的量是衡量物质所含一定数目微观粒子集合体的物理量 | |
| D. | 物质的量的单位--摩尔只适用于微观粒子分子、原子和离子 |
19.下列离子方程式的书写正确的是( )
| A. | NaOH溶液中通入过量的CO2:CO2+2OH-═CO32-+H2O | |
| B. | Fe(NO3)3溶液中加入过量的浓HI溶液:2Fe3++2I-═2Fe2++I2 | |
| C. | 硫酸铝溶液中加入过量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| D. | NaHCO3溶液中加入少量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
6.下列过程或操作变化:①分馏②裂化③裂解④萃取⑤渗析⑥变性⑦盐析其中属于化学变化的是( )
| A. | 只有②③ | B. | ①②⑦ | C. | ①③⑥ | D. | ②③⑥ |
16.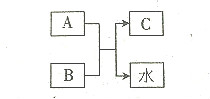 A.B.C均为中学化学常见物质,A、B、C含有同一种元素.且相同的元素不是氢或氧元素.A是一种强酸,B是-种弱碱,C是-种正盐,三者之间的转化关如图所示.则下列说法正确的是.
A.B.C均为中学化学常见物质,A、B、C含有同一种元素.且相同的元素不是氢或氧元素.A是一种强酸,B是-种弱碱,C是-种正盐,三者之间的转化关如图所示.则下列说法正确的是.
 A.B.C均为中学化学常见物质,A、B、C含有同一种元素.且相同的元素不是氢或氧元素.A是一种强酸,B是-种弱碱,C是-种正盐,三者之间的转化关如图所示.则下列说法正确的是.
A.B.C均为中学化学常见物质,A、B、C含有同一种元素.且相同的元素不是氢或氧元素.A是一种强酸,B是-种弱碱,C是-种正盐,三者之间的转化关如图所示.则下列说法正确的是.| A. | C是硝酸盐 | B. | A是硫酸 | C. | B是氢氧化钠 | D. | A的摩尔质量最大 |
19.下列关于化学反应速率的叙述正确的是( )
| A. | 在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值 | |
| B. | 化学反应速率为0.8 mol•L-1•s-1是指1秒钟时某物质的浓度为0.8 mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| D. | 化学反应的速率可以是g•(L•s)-1,也可以是kg•(L•s)-1,甚至可以用t•(L•s)-1表示 |
 下面是硫及其化合物的分类图,请回答下列问题:
下面是硫及其化合物的分类图,请回答下列问题: