题目内容
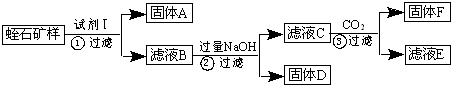
高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列途径制取:

已知NaClO4与NH4Cl投入的物质的量之比为1:1,相关物质的溶解度随温度变化如图所示,下列说法不正确的是( )
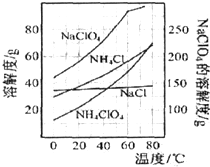

已知NaClO4与NH4Cl投入的物质的量之比为1:1,相关物质的溶解度随温度变化如图所示,下列说法不正确的是( )

| A、制得粗产品的反应原理为:NH4Cl+NaClO4=NaCl+NH4ClO4↓ |
| B、上述流程中操作Ⅰ为冷却结晶,操作Ⅱ为重结晶 |
| C、洗涤粗产品时,宜用冷水洗涤 |
| D、上述流程中蒸发浓缩时,蒸发至剩余少量溶液时,应停止加热,利用余热将其蒸干,防止晶体飞溅 |
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:由图可知,NH4ClO4的溶解度受温度影响很大,NaCl溶解度受温度影响不大,NH4Cl、NaClO4的溶解度受温度影响也很大,但相同温度下,它们溶解度远大于NH4ClO4,故采取蒸发浓缩,冷却结晶可析出高氯酸铵;
通过过滤得到粗产品,进一步得到纯产品,需要经过重结晶.洗涤沉淀时为防止损失,用冷水洗涤.
据此分析判断.
通过过滤得到粗产品,进一步得到纯产品,需要经过重结晶.洗涤沉淀时为防止损失,用冷水洗涤.
据此分析判断.
解答:
解:A.由图可知,NH4ClO4的溶解度受温度影响很大,NaCl溶解度受温度影响不大,NH4Cl、NaClO4的溶解度受温度影响也很大,但相同温度下,它们溶解度远大于NH4ClO4,故采取蒸发浓缩,冷却结晶可析出高氯酸铵;制得粗产品的反应原理为:NH4Cl+NaClO4=NaCl+NH4ClO4↓,符合溶解度大的向溶解度小的方向移动原理,故A正确;
B.通过蒸发浓缩得到过饱和溶液,再降低温度,溶解度小的物质析出,过滤得到粗产品,要得到纯产品,需要经过重结晶,故B正确;
C.由于高氯酸铵的溶解度随温度升高而增大,为了减少高氯酸铵的损失,应用冷水洗涤,故C正确;
D.从流程看,制取高氯酸铵的原理是通过蒸发浓缩冷却结晶的办法,而不是直接蒸发溶液,若蒸干溶液,氯化铵易分解,得到的将是高氯酸钠固体,得不到高氯酸铵粗产品,故D错误;
故选D.
B.通过蒸发浓缩得到过饱和溶液,再降低温度,溶解度小的物质析出,过滤得到粗产品,要得到纯产品,需要经过重结晶,故B正确;
C.由于高氯酸铵的溶解度随温度升高而增大,为了减少高氯酸铵的损失,应用冷水洗涤,故C正确;
D.从流程看,制取高氯酸铵的原理是通过蒸发浓缩冷却结晶的办法,而不是直接蒸发溶液,若蒸干溶液,氯化铵易分解,得到的将是高氯酸钠固体,得不到高氯酸铵粗产品,故D错误;
故选D.
点评:本题以复合火箭推进剂的重要成分制取为背景的综合实验题,涉及理论分析、读图看图、沉淀制备、沉淀洗涤等内容,考查学生对综合实验处理能力,难度较大.注意蒸发和冷却结晶原理不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X、Y和Z三种短周期元素,原子序数之和为32,X和Y为相邻周期的元素,Y和Z为相同周期的元素.Y的质子数比X多5个,X的最外层电子数为Y的最外层电子数的2倍,X的最外层电子数和Z的最外层电子数之和为7,下列叙述中不正确的是( )
| A、X和Y两种元素构成一种阴离子,该阴离子与强酸反应时,可能变成Y的阳离子 |
| B、元素Y的最高价氧化物能溶于Z的最高价氧化物的水化物中 |
| C、X、Y和Z三元素组成的化合物为碱 |
| D、X与Z的单质在不同条件下能生成不同的化合物 |
化学与生产、生活密切相关,下列说法正确的是( )
| A、淀粉溶液、豆浆、雾、碳素墨水均可发生丁达尔现象 |
| B、合金、光导纤维、碳纤维、玻璃钢都属于复合材料 |
| C、明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 |
| D、光化学烟雾、臭氧空洞、温室效应、酸雨(硝酸型)的形成都与氮氧化物有关 |
下列表达方式正确的是( )
| A、乙烯的结构简式CH2CH2 |
B、基态氧原子L层电子排布图: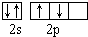 |
C、甲基的电子式 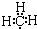 |
| D、HClO的结构式:H-Cl-O |
在0.1mol?L-1的醋酸溶液中,存在电离平衡CH3COOH?CH3COO-+H+,如果要使平衡向逆反应方向移动,同时增大c(H+),应采用的方法是( )
| A、加入0.01 mol?L-1的CH3COOH溶液 |
| B、加入CH3COONa固体 |
| C、稀释 |
| D、加入浓盐酸 |