题目内容
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2
HCOONa+H2O,下列有关说法正确的是( )
| 储氢 |
| 释氢 |
| A、该反应属于可逆反应 |
| B、NaHCO3水溶液的碱性一定比HCOONa水溶液的碱性强 |
| C、储氢过程中,NaHCO3被还原 |
| D、释氢过程中,每转移0.1mol电子放出2.24L的H2 |
分析:A.如反应不在相同条件下进行,则一定不是可逆反应;
B.溶液的碱性取决于溶液的浓度和水解的程度;
C.根据C元素的化合价的变化判断;
D.气体存在的条件未知,不能确定体积关系.
B.溶液的碱性取决于溶液的浓度和水解的程度;
C.根据C元素的化合价的变化判断;
D.气体存在的条件未知,不能确定体积关系.
解答:解:A.储氢和释氢如不在同一条件下进行,则一定不是可逆反应,故A错误;
B.溶液的碱性取决于溶液的浓度和水解的程度,如不在相同浓度下,则无法比较碱性强弱,故B错误;
C.NaHCO3中C元素化合价为+4价,HCOONa中C元素化合价为+2价,储氢过程中,C元素化合价降低,被还原,故C正确;
D.气体存在的条件未知,不能确定体积关系,如是标准状况下,释氢过程中,每转移0.1mol电子放出1.12L的H2,故D错误.
故选C.
B.溶液的碱性取决于溶液的浓度和水解的程度,如不在相同浓度下,则无法比较碱性强弱,故B错误;
C.NaHCO3中C元素化合价为+4价,HCOONa中C元素化合价为+2价,储氢过程中,C元素化合价降低,被还原,故C正确;
D.气体存在的条件未知,不能确定体积关系,如是标准状况下,释氢过程中,每转移0.1mol电子放出1.12L的H2,故D错误.
故选C.
点评:本题考查较为综合,以钠的化合物为载体考查氧化还原反应,侧重于学生的分析能力和自学能力的考查,为高频考点,注意从元素化合价的角度认识,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
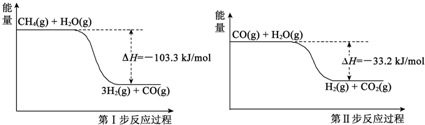 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.