题目内容
5.设NA表示阿伏伽德罗常数的值,下列判断正确的是( )| A. | 将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA | |
| B. | 标准状况下,22.4 L甲醇中含有的C-H的数目为3NA | |
| C. | 25℃时,pH=2的硫酸溶液中,含有的H+的数目为0.01NA | |
| D. | 5.6 g Fe与一定量稀硝酸反应,Fe完全溶解时失去的电子数为3NA |
分析 A、根据溶液的电荷守恒可知:n(NH4+)+n(H+)=n(OH-)+n(NO3-);
B、标况下甲醇为液态;
C、溶液体积不明确;
D、硝酸的量未知,铁最终的化合价不能确定.
解答 解:A、根据溶液的电荷守恒可知:n(NH4+)+n(H+)=n(OH-)+n(NO3-),而溶液显中性,故有:n(H+)=n(OH-),则有:n(NH4+)=n(NO3-)=1mol,故溶液中NH4+数目为NA,
故A正确;
B、标况下甲醇为液态,故不能根据气体摩尔体积来计算其物质的量和C-H键个数,故B错误;
C、溶液体积不明确,故溶液中的氢离子的个数无法计算,故C错误;
D、硝酸的量未知,铁最终的化合价不能确定,故5.6g铁反应后可能全部变为+3价,也肯能过量全部变为+2价,还可能既有+3价又有+2价,故转移的电子数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.某晶体中含有非极性键,关于该晶体的说法正确的是( )
| A. | 可能有很高的熔沸点 | B. | 不可能是化合物 | ||
| C. | 只可能是有机物 | D. | 不可能是离子晶体 |
16. 青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )
青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )
 青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )
青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
20.通过NO传感器可监测NO的含量,其工作原理如图所示.下列说法错误的是( )

| A. | 该装置实现化学能向电能的转化 | |
| B. | 该电池的总反应为2NO+O2═2NO2 | |
| C. | 当有2.24L的O2参与反应时,转移了0.4mole- | |
| D. | NiO电极的电极反应式:NO+O2--2e-═NO2 |
17.生活中处处有化学,下列相关表述正确的是( )
| A. | 苯酚对皮肤有腐蚀性 | B. | 乙醇是不可再生的能源 | ||
| C. | 质量分数100%的酒精为医用酒精 | D. | 天然橡胶的主要成分是异戊二烯 |
14.下列有关化学用语表示正确的是( )
| A. | S2-的结构示意图: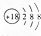 | |
| B. | 质子数为38,中子数为50的Sr原子:5038Sr | |
| C. | NH4Cl的电子式: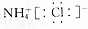 | |
| D. | PBr3的结构式: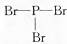 |
1.明星药物青蒿素的分子式为C15H22O5,键线式为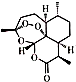 .关于它的说法中,正确的是( )
.关于它的说法中,正确的是( )
 .关于它的说法中,正确的是( )
.关于它的说法中,正确的是( )| A. | 青蒿素是一种氧化物 | |
| B. | 青蒿素中氧元素的质量分数为11.9% | |
| C. | 青蒿素中C、H、O三种元素的质量比为90:11:40 | |
| D. | 青蒿素是由15个碳原子、22个氢原子和5个氧原子构成的 |


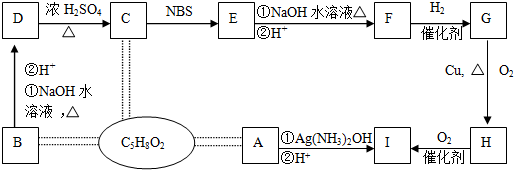
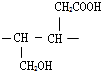 ;
;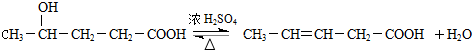 ;
;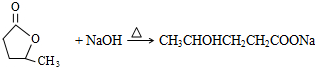 ;
;