题目内容
完成下列填空.
(1)2L 0.5mol/L MgCl2溶液中氯离子的物质的量浓度c(Cl-)= .
(2)16g O2分子的物质的量为 .
(3)标准状况下,11.2L CO2中,氧原子的物质的量n(O)= .
(4)2mol Fe2(SO4)3中,有 个SO42-.
(5)标况下3.36L HCl气体溶于水,配成500ml溶液,求该溶液中溶质的物质的量浓度c(HCl)= .
(1)2L 0.5mol/L MgCl2溶液中氯离子的物质的量浓度c(Cl-)=
(2)16g O2分子的物质的量为
(3)标准状况下,11.2L CO2中,氧原子的物质的量n(O)=
(4)2mol Fe2(SO4)3中,有
(5)标况下3.36L HCl气体溶于水,配成500ml溶液,求该溶液中溶质的物质的量浓度c(HCl)=
考点:物质的量的相关计算,物质的量浓度的相关计算
专题:计算题
分析:(1)c(Cl-)=2c(MgCl2);
(2)结合n=
的计算;
(3)结合n=
及分子构成计算;
(4)结合N=nNA及分子构成计算;
(5)结合n=
、c=
计算.
(2)结合n=
| m |
| M |
(3)结合n=
| V |
| Vm |
(4)结合N=nNA及分子构成计算;
(5)结合n=
| V |
| Vm |
| n |
| V |
解答:
解:(1)0.5mol/L MgCl2溶液中氯离子的物质的量浓度c(Cl-)=0.5mol/L×2=1mol/L,故答案为:1mol/L;
(2)16g O2分子的物质的量为
=0.5mol,故答案为:0.5mol;
(3)标准状况下,11.2L CO2中,物质的量为
=0.5mol,氧原子的物质的量n(O)=0.5mol×2=1 mol,故答案为:1mol;
(4)2mol Fe2(SO4)3中,n(SO42-)=2mol×3=6mol,则离子个数为6NA,故答案为:6NA;
(5)标况下3.36L HCl,n(HCl)=
=0.15mol,配成500ml溶液,该溶液中溶质的物质的量浓度c(HCl)=
=0.3mol/L,故答案为:0.3mol/L.
(2)16g O2分子的物质的量为
| 16g |
| 32g/mol |
(3)标准状况下,11.2L CO2中,物质的量为
| 11.2L |
| 22.4L/mol |
(4)2mol Fe2(SO4)3中,n(SO42-)=2mol×3=6mol,则离子个数为6NA,故答案为:6NA;
(5)标况下3.36L HCl,n(HCl)=
| 3.36L |
| 22.4L/mol |
| 0.15mol |
| 0.5L |
点评:本题考查物质的量的计算,为高频考点,把握以物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的综合考查,题目难度不大.

练习册系列答案
相关题目
下列试剂的保存或使用正确的是( )
| A、实验室的氯水需要保存在棕色试剂瓶中 |
| B、漂白粉比氯水稳定,可露置在空气中 |
| C、称量氢氧化钠固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码 |
| D、金属钠可保存在煤油、四氯化碳等有机溶剂中 |
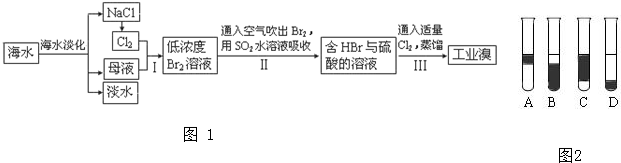
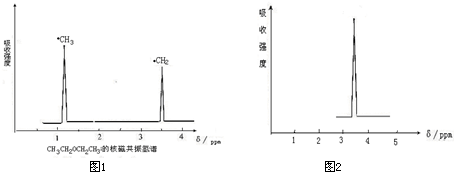
 (1)铁、铝、铜是人类使用广泛的三种金属.
(1)铁、铝、铜是人类使用广泛的三种金属.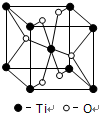
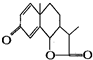 是一种驱虫药--山道年的结构简式.试确定其分子式为
是一种驱虫药--山道年的结构简式.试确定其分子式为