题目内容
在2008年国际奥林匹克化学竞赛中,某兴趣小组在“探究卤素单质的氧化性”的实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
为此提出问题:Fe3+、Br2谁的氧化性更强?
(1)猜想
①澳大利亚代表团同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含________(填化学式,下同)所致。
②美国代表团同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含________所致。
(2)设计实验并验证
为验证美国代表团同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了美国代表团同学的观点确实是正确的。
可以选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 |
方案1 |
|
|
方案2 |
|
|
(3)结论
氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为________________________________________________
(4)依据上述结论,向FeBr2溶液中通入等量Cl2,写出该反应的离子方程式: 。
(1)Br2、Fe3+;(2)方案1、2可互换选用试剂实验现象,方案1:b CCl4层呈无色;方案2:d 溶液变红色;(3)2Fe2++Br2=2Fe3++2Br—;(4)2Fe2++2Br—+2Cl2=2Fe3++ Br2+4Cl—;
【解析】试题分析:①澳大利亚代表团同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含Br2的缘故;②美国代表团同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,发生反应是:2Fe2++Br2=2Fe3++2Br—;则溶液呈黄色是含Fe3+所致。(2) 方案1:选择试剂b,若 CCl4层呈无色就证明黄色是Fe3+所致,澳大利亚代表团错误,美国代表团正确;方案2:选择试剂d.KSCN溶液,若溶液变红色,就证明溶液显黄色是Fe3+所致,同样可以证明澳大利亚代表团错误,美国代表团正确;(3)结论氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为2Fe2++Br2=2Fe3++2Br—;(4)依据上述结论,向FeBr2溶液中通入等量Cl2,则该反应的离子方程式是2Fe2++2Br—+2Cl2=2Fe3++ Br2+4Cl—。
考点:考查物质反应的先后顺序、试剂的选择、检验方法、实验现象、离子方程式的书写的知识。

 阅读快车系列答案
阅读快车系列答案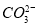 的实验事实是 ( )
的实验事实是 ( ) Fe3O4 B.C+ O2
Fe3O4 B.C+ O2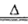 2CO
2CO 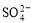 离子有一部分是氧化产物
离子有一部分是氧化产物  5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37
5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37