题目内容
18.下列操作中,不会发生明显颜色变化的是( )| A. | FeSO4溶液中滴加NaOH浓液 | B. | 碳酸氢钠溶液中滴加稀盐酸溶液 | ||
| C. | 硫酸铁溶液中滴加硫氰化钾溶液 | D. | 氯化铁溶液中加入还原性铁粉 |
分析 A.FeSO4溶液中滴入NaOH溶液,生成白色沉淀,迅速变为灰绿色,最后变为红褐色;
B.溶液无色,生成二氧化碳气体;
C.硫酸铁溶液中滴加硫氰化钾溶液生成血红色溶液;
D.氯化铁溶液中加入还原性铁粉反应生成氯化亚铁,溶液由黄色变为浅绿色.
解答 解:A.FeSO4溶液中滴入NaOH溶液反应,Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,发生颜色变化,故A不选;
B.溶液无色,生成二氧化碳气体,没有颜色变化,故B选;
C.硫酸铁溶液中滴加硫氰化钾溶液生成硫氰酸铁,溶液由黄色变为血红色溶液,Fe3++3SCN-=Fe(SCN)3,发生颜色变化,故C不选;
D.氯化铁溶液中加入还原性铁粉发生反应Fe+2Fe3+=3Fe2+,溶液从黄色变为浅绿色,发生颜色变化,故D不选.
故选B.
点评 本题考查铁及其化合物的性质、钠的化合物的性质应用,为高频考点,侧重于学生的分析能力的考查,明确发生的化学反应来分析溶液颜色的变化即可解答.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
8.下列各物质所含分子数目最多的是( )
| A. | 0.5mol NH3 | B. | 标准状况下22.4L He | ||
| C. | 100ml 10%的食盐水 | D. | 147g H2SO4 |
9.下列关于电解质的说法正确的是( )
| A. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 | |
| B. | 水溶液中导电能力差的电解质一定是弱电解质 | |
| C. | 在稀的水溶液中,强电解质近乎全部以离子的形态存在,一定不存在电解质分子 | |
| D. | 强电解质都是离子化合物,而弱电解质都是共价化介物 |
6.将1.85g含锌、铁、铜的合金放入足量的盐酸中,反应完毕后,得448mL(标况)氢气,关于此合金的组成,下列说法中不正确的是( )
| A. | 合金中铁、锌的物质的量之和为0.02mol | |
| B. | 合金中铜的质量无法确定 | |
| C. | 合金中铁、铜的物质的量之和为0.01mol | |
| D. | 1.30g>铁和锌质量之和>1.12g |
13.氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁.实验室制备装置和工业制备流程图如图:
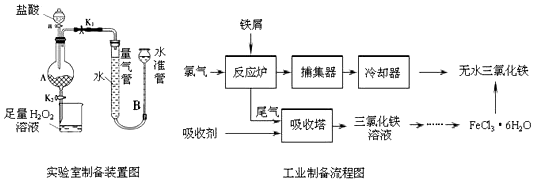
已知:(1)无水FeCl3的熔点为555K、沸点为588K.
(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如表:
实验室制备操作步骤如下:
Ⅰ打开弹簧夹K1,关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ当装置A中不产生气泡或量气管和水准管液面不变时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体.
请回答:
(1)烧杯中足量的H2O2溶液的作用是把亚铁离子全部氧化成三价铁离子.
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是装置A中不产生气泡或量气管和水准管液面不变.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入盐酸后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为Fe2Cl6.
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-═2I-+S4O62-).
①滴定过程中可能造成实验结果偏低的是BC
A.锥形瓶未润洗 B.锥形瓶中溶液变色后立刻停止滴定,进行读数
C.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡 D.滴定终点时仰视读数
②$\frac{162.5cV}{m}%$样品中氯化铁的质量分数.

已知:(1)无水FeCl3的熔点为555K、沸点为588K.
(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如表:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
Ⅰ打开弹簧夹K1,关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ当装置A中不产生气泡或量气管和水准管液面不变时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体.
请回答:
(1)烧杯中足量的H2O2溶液的作用是把亚铁离子全部氧化成三价铁离子.
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是装置A中不产生气泡或量气管和水准管液面不变.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入盐酸后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为Fe2Cl6.
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-═2I-+S4O62-).
①滴定过程中可能造成实验结果偏低的是BC
A.锥形瓶未润洗 B.锥形瓶中溶液变色后立刻停止滴定,进行读数
C.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡 D.滴定终点时仰视读数
②$\frac{162.5cV}{m}%$样品中氯化铁的质量分数.
3.化学与生活、社会发展细细相关,下列有关说法不正确的是( )
| A. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| B. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| D. | 维生素C具有还原性,在人体内起抗氧化作用 |
1.下列反应的离子方程式书写错误的是( )
| A. | 新制氯水和溴化钾溶液反应:Cl2+2Br-═2Cl-+Br2 | |
| B. | 碳酸钙和稀盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 盐酸和氢氧化钠溶液反应:H++OH-═H2O | |
| D. | 铝和氢氧化钠溶液反应:Al+2H2O+OH-═AlO2-+2H2↑ |

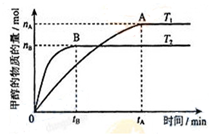 甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下
甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下 .
.