��Ŀ����
4��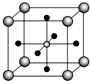 ������������Խ������Ϊ��Fe��Al��Ӧ�ù㷺�ġ�������������
������������Խ������Ϊ��Fe��Al��Ӧ�ù㷺�ġ���������������1��Ti��̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p63d24s2��
��2��������B��C��N��O�ȷǽ���Ԫ���γ��ȶ��Ļ�����縺�ԣ�C�����������������ͬ��B����һ�����ܣ�N��O��ԭ����Nԭ���е�2p������ڰ����״̬�����ȶ���
��3��������ʯ--�����ҵ���Ҫ�ɷ�Ϊ����������FeTiO3����FeTiO3��80%�����ᷴӦ������TiOSO4��SO42-�Ŀռ乹��Ϊ���������Σ�������ԭ�Ӳ���sp3�ӻ���д��SO42-��һ�ֵȵ�����Ļ�ѧʽ��ClO4-�ȣ�
��4��Ti���������CaO��������γ�������CaTiO3��CaTiO3�ľ���ṹ��ͼ��ʾ��Ti4+λ��������Ķ��㣩���þ����У�Ti4+����Χ12��O2-����ڣ�
��5��Fe���γɶ������������FeO�����ṹΪNaCl�ͣ�������ʵ���ϴ��ڿ�λ����λ������ԭ�ӵ�ȱ�ݣ�����ȱ�ݶԾ�������ʻ�����ش�Ӱ�죮���ھ���ȱ�ݣ��ھ�����Fe��O�ĸ����ȷ����˱仯����ΪFexO��x��1���������ijFexO�����ܶ�Ϊ5.71g•cm-3�������߳�Ϊ4.28��10-10 m����FexO��x=$\frac{{N}_{A}��5.71����4.28��1{0}^{-8}��^{3}}{4��56}$-$\frac{16}{56}$���ô���ʽ��ʾ����Ҫ���������������
���� ��1��Tiԭ�Ӻ��������Ϊ22�������������ԭ����д��������Ų�ʽ��
��2��ͬ�����������Ԫ�ص縺������Nԭ���е�2p������ڰ����״̬�����ȶ�����һ�����ܸ���ͬ��������Ԫ�صģ�
��3��SO42-��Sԭ�ӹµ��Ӷ���=$\frac{6+2-2��4}{2}$=0���۲���Ӷ���=4+0=4���ӻ������ĿΪ4���ݴ�ȷ���ռ乹�����ӻ���ʽ��ԭ����Ŀ��ͬ���۵���������ͬ������Ϊ�ȵ����壻
��4��CaTiO3�ľ���ṹ��Ti4+λ��������Ķ��㣬�ɾ����ṹͼ��֪������ΪCa2+������ΪO2-���þ�����ÿ������Ti4+�����ĵ�O2-���ڣ�ÿ������Ϊ8���������ã�ÿ����Ϊ2���������ã�
��5��FexO����ľ����ṹΪNaCl�ͣ�����ÿ�������к���4��Oԭ�ӣ���4����FexO�����ٸ���m=��V���㣮
��� �⣺��1��Tiԭ�Ӻ��������Ϊ22�������������ԭ������������Ų�ʽΪ��1s22s22p63s23p63d24s2��
�ʴ�Ϊ��1s22s22p63s23p63d24s2��
��2��ͬ�����������Ԫ�ص縺�����ʵ縺��C��B��Nԭ���е�2p������ڰ����״̬�����ȶ�����һ�����ܸ���ͬ��������Ԫ�صģ��ʵ�һ������N��O��
�ʴ�Ϊ����������Nԭ���е�2p������ڰ����״̬�����ȶ���
��3��SO42-��Sԭ�ӹµ��Ӷ���=$\frac{6+2-2��4}{2}$=0���۲���Ӷ���=4+0=4��Ϊ��������ṹ���ӻ������ĿΪ4��Sԭ���ӻ���ʽΪsp3��ԭ����Ŀ��ͬ���۵���������ͬ������Ϊ�ȵ����壬SO42-��һ�ֵȵ�����Ļ�ѧʽ��ClO4-�ȣ�
�ʴ�Ϊ���������壻sp3��ClO4-�ȣ�
��4��CaTiO3�ľ���ṹ��Ti4+λ��������Ķ��㣬�ɾ����ṹͼ��֪������ΪCa2+������ΪO2-�������þ�����ÿ������Ti4+�����ĵ�O2-���ڣ�ÿ������Ϊ8���������ã�ÿ����Ϊ2���������ã������У�Ti4+����Χ������O2-��ĿΪ$\frac{3��8}{2}$=12��
�ʴ�Ϊ��12��
��5��FexO����ľ����ṹΪNaCl�ͣ�����ÿ�������к���4��Oԭ�ӣ���4����FexO�����ٸ���m=��V��֪��4��$\frac{56x+16}{{N}_{A}}$g=5.71g•cm-3����4.28��10-8 cm��3����ã�x=$\frac{{N}_{A}��5.71����4.28��1{0}^{-8}��^{3}}{4��56}$-$\frac{16}{56}$��
�ʴ�Ϊ��$\frac{{N}_{A}��5.71����4.28��1{0}^{-8}��^{3}}{4��56}$-$\frac{16}{56}$��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų����縺�ԡ������ܡ��ռ乹�����ӻ���ʽ�жϡ��ȵ����塢�����ṹ����㣬��5���м���Ϊ�״��㡢�ѵ㣬ע��ʶ����ѧ���������ṹ���Ѷ��еȣ�

| A�� | ������SO2��NO��N2��NH3 | |
| B�� | 0.1mol/L��NaNO3��Һ�У�K+��I-��Cl-��SO42- | |
| C�� | ����ϡ���ᷴӦ�����Һ�У�[Fe��CN��6]3-��NH4+��Cl-��NO3- | |
| D�� | ������Ӧ���ɴ�����������Һ�У�Mg2+��K+��HCO3-��NO3- |
| A�� | �ı���������Ӧ���ת��������ƽ�ⳣ��Ҳһ������ | |
| B�� | �����£�V1L pH=12��NaOH��Һ��V2L pH=2��HA��Һ��ϣ������Һ�����ԣ���V1��V2 | |
| C�� | ��0.1mol•L-1 NaHCO3��Һ�У���������NaOH���壬Na+��CO32-������Ũ�Ⱦ����� | |
| D�� | ��Ӧ2NO2��g��?N2O4��g����H��O�������¶ȸ÷�Ӧƽ�ⳣ������ |
| A�� | �κ�����Ӧ����1 mol H2O�Ĺ����У��ų�����������ͬ | |
| B�� | �������������������ֱ���ȫȼ�գ�ǰ�߷ų������� | |
| C�� | ����ʱ��H2��g��+Cl2��g���T2HCl��g����H=aKJ/mol������Ӧ������Ϊ��ȼ����H������ | |
| D�� | ��ʾ̼ȼ���ȵ��Ȼ�ѧ����ʽΪ��2C��s��+O2��g���T2CO��g����H=-221kJ•mol-1 |
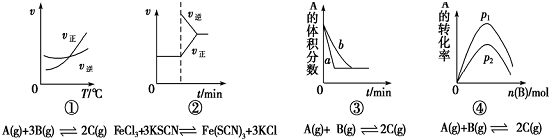
| A�� | ͼ������������һ��ʱ��Ӧ�������¶ȱ仯��ͼ��ͼ��������ϵ��¶�������ƽ�������ƶ����ϸ��¶�������ƽ�������� | |
| B�� | ͼ������ƽ����ϵ����Һ�м�������KCl�����ѧ��Ӧ������ʱ��ı仯 | |
| C�� | ͼ�ۿ����Ǵ����Ի�ѧƽ���Ӱ�죬Ҳ�������������ضԻ�ѧƽ���Ӱ�� | |
| D�� | ͼ����һ�������£�����һ����A������������Bʱ��ͼ��ѹǿp1��p2 |

| A�� | �����к���4�ֹ����� | |
| B�� | ����ʽΪC10H8O6 | |
| C�� | 1mol��֦��������2mol�Ҵ�����������Ӧ | |
| D�� | ��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ����ԭ����ͬ |
| ������Ϊ���� | �����Լ� | ���Ӳ��� | |
| A | Na2O2��Na2O�� | O2 | �ڴ����м��� |
| B | Na2CO3��NaHCO3�� | CO2 | ͨ�������CO2 |
| C | FeCl��FeCl2�� | Cl2 | ͨ�������Cl2 |
| D | FeSO4��CuSO4�� | Fe | ���������Fe�ۣ���ַ�Ӧ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��ϩʹ��ˮ��ɫ | B�� | �Ҵ���Ũ���Ṳ����170�� | ||
| C�� | ��������NaOHˮ��Һ���� | D�� | ��Һ���뱽�Ļ�������������� |