题目内容
下列微粒:①H3O+②[Cu(NH3)4]2+ ③CH3COO- ④NH3 ⑤CH4 ⑥CO中存在配位键的是( )
| A、①②③ | B、①③④ |
| C、④⑤⑥ | D、①②⑥ |
考点:配合物的成键情况
专题:
分析:在物质或离子中中心原子含有空轨道,和含有孤电子对的原子或离子能形成配位键,
①氢离子提供空轨道,氧原子提供孤电子对;
②铜离子提供空轨道,氮原子提供孤电子对;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对;
④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;
⑤CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键,无空轨道,无孤电子对;
⑥CO为共价化合物,分子中氧提供孤电子对,碳提供空轨道.
①氢离子提供空轨道,氧原子提供孤电子对;
②铜离子提供空轨道,氮原子提供孤电子对;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对;
④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;
⑤CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键,无空轨道,无孤电子对;
⑥CO为共价化合物,分子中氧提供孤电子对,碳提供空轨道.
解答:
解:解:①H3O+中O提供孤电子对,H+提供空轨道,二者形成配位键,H3O+含有配位键;
②Cu2+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,[Cu(NH3)4]2+ 含有配位键;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对,电子式为: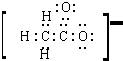 ,不含有配位键;
,不含有配位键;
④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;
⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为 ,无空轨道,无孤电子对,CH4不含有配位键;
,无空轨道,无孤电子对,CH4不含有配位键;
⑥CO为共价化合物,分子中氧提供孤电子对,碳提供空轨道,故选D.
②Cu2+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,[Cu(NH3)4]2+ 含有配位键;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对,电子式为:
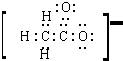 ,不含有配位键;
,不含有配位键;④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;
⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为
 ,无空轨道,无孤电子对,CH4不含有配位键;
,无空轨道,无孤电子对,CH4不含有配位键;⑥CO为共价化合物,分子中氧提供孤电子对,碳提供空轨道,故选D.
点评:本题考查配位键的判断,明确配位键的形成是解本题关键,题目难度中等.注意配位键形成的条件,一方要提供空轨道,另一方提供孤电子对.

练习册系列答案
相关题目
在下列物质中,其物质的量为0.2mol的是( )
| A、2.2g CO2 |
| B、3.6g H2O |
| C、3.2g O2 |
| D、49g H2SO4 |
以下实验装置一般不用于分离物质的是( )
A、 |
B、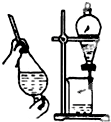 |
C、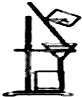 |
D、 |
常温下,将pH=3的盐酸与pH=9的Ba(OH)2溶液混合,若要得到pH=7的溶液,混合时盐酸与Ba(OH)2溶液的体积比为( )
| A、1:60 | B、3:1 |
| C、100:1 | D、1:100 |
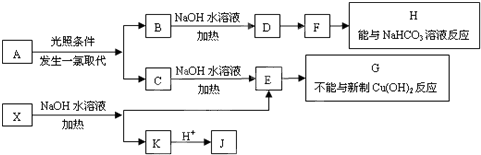
 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.